Cell dive超多标助力 --牛津团队仅凭4个样本砸百万做空转,活体亚细胞空间组学重塑研发范式
知识背景板:Leica Cell DIVE vs. 传统多重免疫荧光(mIF)
传统免疫荧光(IF)/ 常规 mIF:受限于荧光通道和光谱重叠,往往只能在切片上截取几个局部视野(FOV)。
Cell DIVE(全切片多重荧光成像系统):Cell DIVE 系统通过循环成像,可在整张全切片上原位检测 60 种以上的蛋白。
在单细胞测序(scRNA-seq)越来越追求样本量的今天,发表顶刊似乎动辄需要成百上千个病人的数据。抛出五六百万细胞的图谱,已成为工业界和学术界的标配。
然而,近期“药研逻辑”在追踪前沿文献时,偶然发现了牛津大学团队刚刚在生物学预印本平台 bioRxiv 上发表的一篇巨作:《Machine perfusion and single-cell spatial transcriptome mapping identifies novel immune escape mechanisms in colorectal cancer liver metastasis》。看完之后,其研究思路彻底颠覆了常规认知,非常值得业界学习。

这是一项针对结直肠癌肝转移(CRLM)的重磅研究。团队摒弃了常规的大样本解离测序和动物模型,利用极其罕见的人类离体活器官常温灌流,结合亚细胞级空间组学,完成了一次真正意义上的活体空间免疫追踪。他们史无前例地在人类真实器官层面,原位证实了内皮细胞失能(Endothelial anergy)与应激态 T 细胞(CD4-Tstr)这两大前沿概念。
令人震惊的是,其核心的空间转录组仅仅测了 4 个病人,且没有设置常规的健康人对照组。
审稿人可能会质疑,在人类样本至少要求 3v3、鼠源样本至少 6v6 才能发文章的当下,区区 n=4 的样本量,凭什么代表微环境的异质性?作者怎么敢在这上面砸上百万的测序费用?
但这正是这篇文章的绝妙之处,它打破了唯样本量论与结果堆砌的生信内卷。为了看懂这篇巨作,我们不妨先解构作者构建的这套多维数据矩阵。
文章中所使用数据
活体功能与流式验证:成功运行 3 例人类离体活器官常温机械灌流(NMP)模型,并通过流式细胞术(FACS)对配对的肿瘤与肝脏组织进行了 T 细胞渗出率的精准量化。
亚细胞分辨率的空间深度:4 例高度同质化的微卫星稳定型(MSS)、替换型生长且接受过新辅助化疗的 CRLM 组织样本生产 193 万 个带绝对坐标的单细胞(PS:通过极致的控制变量,消除个体遗传背景差异)。
全切片多重免疫荧光的空间广度:13 例 MSS 型 CRLM 及匹配背景肝脏的全切片样本(Cell DIVE),检测出 1000万+ 细胞,识别 23 种细胞类型。
外部独立验证增加普适性:整合两大独立公开单细胞测序数据集(E-MTAB-12022 与 phs001818.v3.p1,包含未经化疗等更广泛真实世界基线的 CRLM 及配对肝脏样本),进行严苛的外部交叉验证。
今天,“药研逻辑”带您硬核拆解这篇极具爆款潜力的巨作,通过四大核心维度,看看顶尖团队是如何以小见大,重塑微环境研究思路的。
一、 技术降维打击:在人类离体活器官上跑通动态免疫追踪
寻找免疫细胞无法进入肿瘤的真相,最强大的武器是动态活体追踪。但常规的静态切片只能观察死细胞位置,而鼠源模型又缺乏人类微环境的真实度,这些方法在复杂的实体瘤屏障面前宛如隔靴搔痒。此外,类器官(Organoids)虽发展迅猛,但因缺乏真实的血管网络和免疫空间信息,远没有在体外直接复活一个人类脏器 24 小时来得震撼。牛津团队在这里实现了硬核突破。
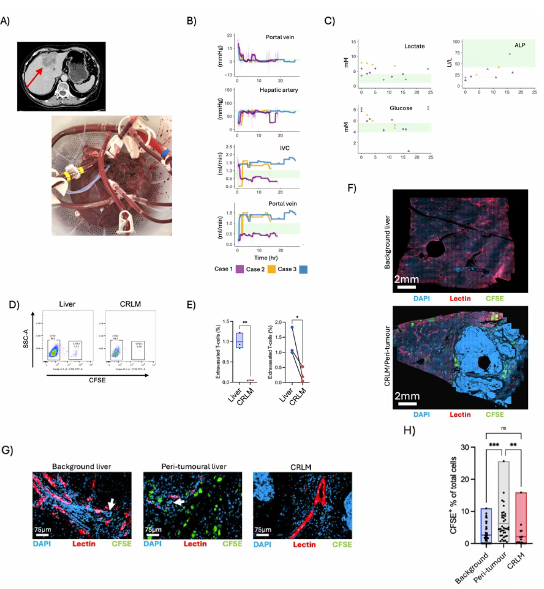
Fig. 1. T 细胞在结直肠癌肝转移(CRLM)中渗出失败
团队首先利用 OrganOx metra 灌流设备,将手术切除的包含 CRLM 的人类半肝重新接通血管,在 37°C 下维持正常的血液动力学与肝功能,让真实的人类脏器在体外存活了 24 小时(Fig. 1A-1C)。这就是文章点睛之笔,人类离体活器官常温机械灌流(NMP)。
PS:亮点(影像与流式的双重金标准铁证):团队成功向这条真实的活体血管网络中注入了荧光标记的 T 细胞。为了证明 T 细胞真的进不去肿瘤,作者给出了两项核心证据。
利用高分辨共聚焦显微成像(Confocal Microscopy)直观高精度识别。通过血管内皮标志物(CD31)与荧光 T 细胞的三维共定位,史无前例地绘制出了 T 细胞渗出(Extravasation)的动态图谱(Fig. 1D-1F)。
利用流式细胞术(FACS)给出定量数据。为了排除切片成像的局部取样偏差,团队直接将灌流后的正常肝脏与肿瘤组织彻底解离,用 FACS 进行全景分析。数据证实,T 细胞在正常肝脏和瘤周都能顺利穿过血管壁,但在 CRLM 肿瘤核心区的渗出率却呈现出断崖式的骤降(Fig. 1G-1H)。
共聚焦看位置,流式数人头。这就是铁证:并非 T 细胞不作为,而是肿瘤根本不让进。
知识背景板:人类离体活器官 NMP vs. 动物模型/类器官
寻找免疫逃逸机制,为什么非要用这么昂贵的器官复活技术?
动物模型(PDX/CDX):老鼠的基质和血管内皮结构与人类差异巨大,人类的物理屏障远远大于小鼠,而且缺乏真实的人类免疫系统互作。得出的结论往往是“在老鼠身上大杀四方,一上临床全军覆没”。
类器官(Organoids)/ 器官芯片:近些年 FDA 批准类器官可以替代动物实验,类器官虽前沿,但其致命伤在于缺乏真实的血管网络(无血压、无真实的血液动力学剪切力)与宏观的免疫空间纵深。
- 人类离体活器官 NMP:保留了最真实的物理城墙(内皮屏障)。它能让我们像看监控录像一样,亲眼看着 T 细胞在真实的血管里“撞墙”,这种震撼力和临床转化价值是体外模型完全无法比拟的。
二、 机制破解:内皮“失能”是阻碍免疫的“物理叹息之墙”
工业界的痛点在于,如果不知道是什么分子锁死了血管,就无法开发增敏药物。肿瘤究竟是如何在分子层面让血管内皮拒绝通行的?
确认了现象,接下来要找分子机制。作者祭出了新一代亚细胞级空间转录组 CosMx SMI (6K Panel)。只有 4 个病人,且没有健康对照,怎么规避个体差异?作者极其聪明地利用了空间内参逻辑,在同一张切片上对比肿瘤核心、瘤周边缘与正常远端,让每个病人都成为自己的完美对照。
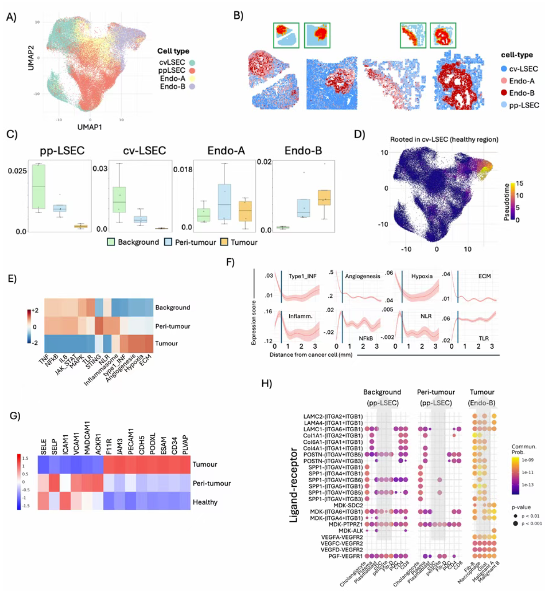
Fig. 3. CRLM 内皮细胞的“失能(Anergy)”状态
传统空转(如 10x Visium)一个测序点(Spot)里往往挤着十几个甚至几十个细胞,需要拿普通的单细胞数据做复杂的解卷积(Deconvolution)去盲猜比例。这就像拿到一杯打碎的混合果汁,硬猜里面有几个苹果。
而本文的数据证实,肿瘤内部的内皮细胞(Endo-B)与正常肝脏内皮在转录组上截然不同,呈现出连续的演化轨迹(Fig. 3A-3D)。通过计算细胞到肿瘤核心的绝对物理距离,团队完美拟合出了内皮细胞炎症评分从正常、瘤周再到肿瘤内部的连续衰减曲线(Fig. 3E-3F)。
PS:亮点(无解卷积的亚细胞级空转):结合 CosMx 平台与 CellPose 算法精准勾勒出的 193 万个单细胞边界,团队揭示了内皮细胞的失能(Anergy)本质。它不仅强力下调了负责抓取 T 细胞的粘附分子(如 SELP、VCAM1),更是显著上调了维持物理屏障的基因(如 PECAM1、CDH5)(Fig. 3G)。Fig. 3H 的通讯图清晰展示了基质细胞如何通过 VEGF 和胶原蛋白强制内皮细胞维持在恶性的封闭状态。这在分子层面完美解释了活体灌流中 T 细胞被挡在血管内、无法进入肿瘤组织的真相。
三、 “阵地粉碎”的铁证:基质内鬼对免疫防线的物理强拆
内皮城墙建立后,那些侥幸在城外(瘤周)下车的免疫军队,是否还能维持阵地?
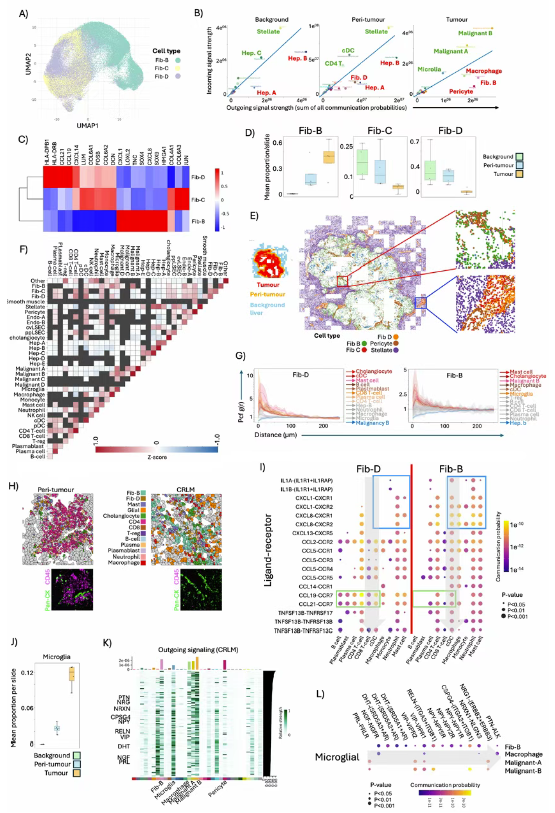
Fig. 4. CRLM 与背景肝脏中的成纤维细胞可塑性
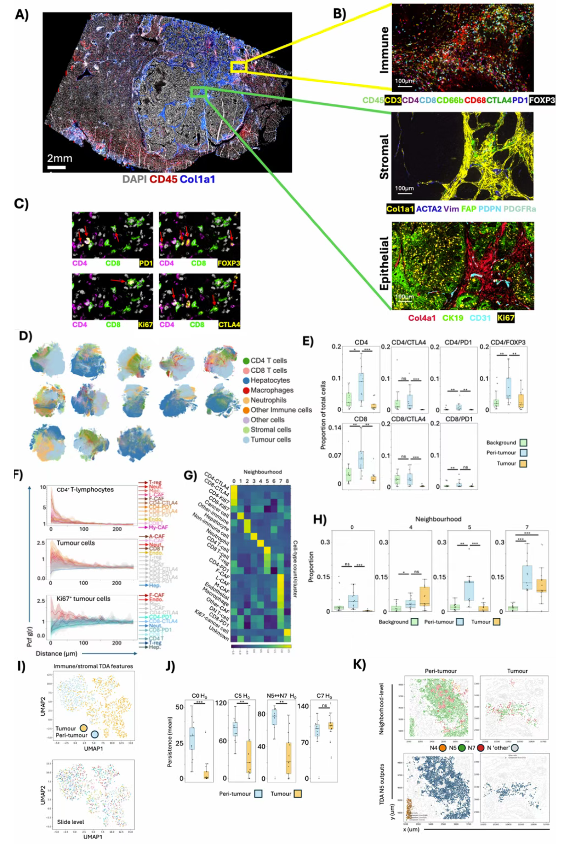
Fig. 5. 瘤周肝脏中高度组织化的细胞耗竭微环境
空间通讯分析(CellChat)证实,负责维持这些淋巴结构的成纤维细胞(Fib-D)在肿瘤内部彻底消失,取而代之的是疯狂招募巨噬细胞的 Fib-B 亚型,以及罕见的小胶质细胞(Microglia)(Fig. 4F-4L)。
此外,在 Cell DIVE 千万级细胞(13 个全切片标本)的多重免疫荧光模型中,T 细胞确实被死死挡在了肿瘤外部,只能在瘤周形成密集的淋巴聚集区(Fig. 5A-5E)。
PS:亮点(拓扑数据分析 TDA 重建战场):团队没有用低级的数细胞个数来量化,而是引入了极具降维打击感的拓扑数据分析(TDA)。算法将 1000 万个细胞视为城市建筑,证实了肿瘤基质的扩张彻底打断了 T 细胞之间极其关键的物理连接。原本紧密相连的防御社区(N5 结构)被像推土机一样无情地碾碎成了互不相通的孤岛(Fig. 5G-5K)。T 细胞不仅进不了城,连城外的营地都被物理强拆了。
传统免疫荧光(IF)/ 常规 mIF:受限于荧光通道和光谱重叠,往往只能在切片上截取几个局部视野(FOV)。
Cell DIVE(全切片多重荧光成像系统):Cell DIVE 系统通过循环成像,可在整张全切片上原位检测 60 种以上的蛋白。
四、 概念颠覆与平反:极度缺氧驱动的应激态 T 细胞
少数侥幸钻进肿瘤核心的 T 细胞,究竟能不能成为下一代细胞疗法(如 TIL)或抗体偶联药物(ADC)的新基石?
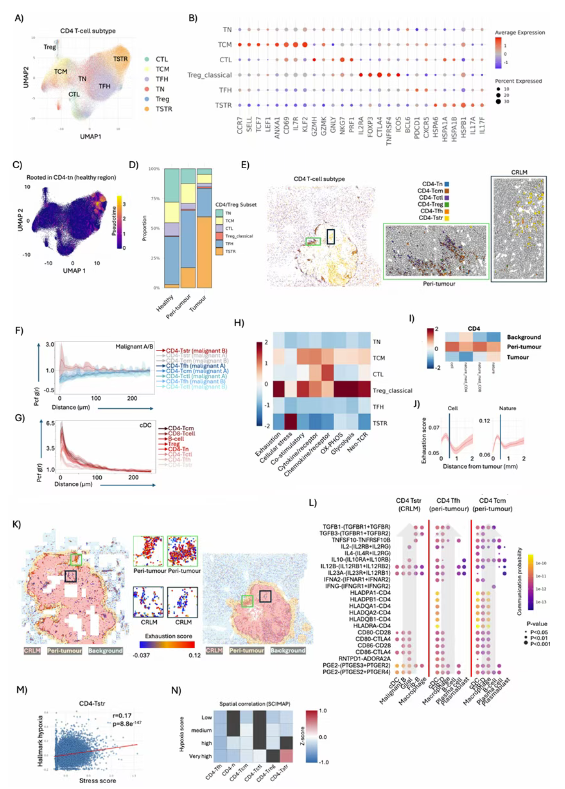
Fig. 6. CRLM 及瘤周肝脏中 CD4+ T 细胞的功能障碍与应激
基于 CosMx 亚细胞级空间原位数据的聚类显示,停留在瘤周的 CD4+ T 细胞表现出极高的耗竭(Exhaustion)特征(Fig. 6I-6K),但仍保留一定的 TCR 反应性。但当视线转移到极少数进入肿瘤内部的 T 细胞时,发生了奇特的变化:它们异化为一种高表达热休克蛋白(HSPA1A/B)的应激态(CD4-Tstr),彻底丧失了抗癌功能(Fig. 6A-6H)。
PS:亮点(原位冻结的空间防伪):在过去的单细胞研究中,这类高表达 HSP 的细胞往往被当成酶消化导致的实验伪影而剔除。但团队利用未解离的原位空转数据,史无前例地为这群细胞平反。空间关联分析(SCIMAP)给出了强力证据,这些 CD4-Tstr 细胞死死地钉在肿瘤核心最缺氧的角落,且其单细胞缺氧(Hypoxia)评分与应激评分呈现出极其完美的正相关(Fig. 6M-6N)。这证明,是微环境的毒气而非实验操作,将 T 细胞逼入了绝境。
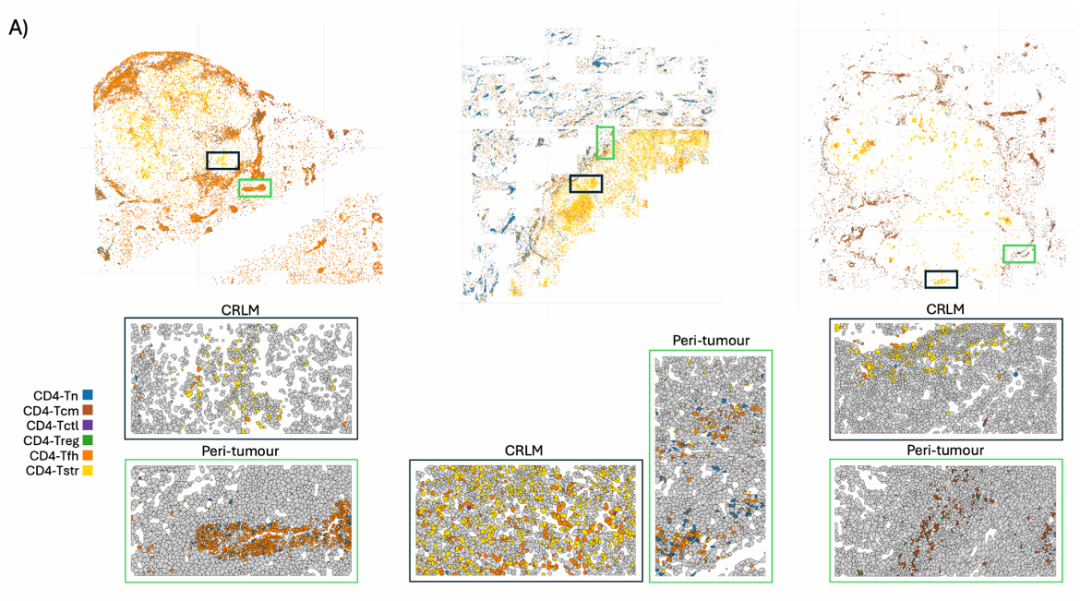
Supp Fig. 10A. 跨组织的 T 细胞耗竭与表型状态空间映射
此外,我们直观地看到,这些 CD4-Tstr 细胞并不是随机分布的,它们的物理坐标死死地钉在肿瘤核心(CRLM)最缺氧的角落(Supp Fig. 10A)。通过亚细胞级别的量化分析,为 CD4-Tstr 提供了确凿的物理铁证。
知识背景板:耗竭态 T 细胞(Exhaustion) vs. 应激态 T 细胞(Stress)
耗竭态 T 细胞(Exhaustion):因长期抗原刺激导致“累趴下”,常见于瘤周,往往是 PD-1 抑制剂(IO 疗法)试图唤醒的对象。
应激态 T 细胞(Stress):不像耗竭态 T 细胞,刚开始应激态 T 细胞出来的时候,因为它的 marker 是热休克蛋白,许多研究者质疑,这可能是因为单细胞悬液制备时实验操作不当产生的伪影。小编也曾是质疑的一员,直到近期看到了这篇文章的空间原位证据。这些想法在近期 Nature 上《Proteotoxic stress response drives T cell exhaustion and immune evasion》定义的蛋白毒性应激(Tex-PSR)机制中得到了更深刻的验证。因极度缺氧和化学压迫(如 PGE2)导致内部蛋白质折叠崩溃,彻底丧失 TCR 反应性。这完美解释了为何强行用检查点抑制剂,也根本无法唤醒核心区的 T 细胞。
结语:重塑“微环境重编程”的研发范式
这项工作跳出了传统的配体-受体通路思维,转向了更加宏大的空间物理学视角。为了让大家更直观地理解,我们可以把结直肠癌肝转移的微环境想象成一座戒备森严的中世纪城堡,而 T 细胞是试图攻城的军队。这篇大作揭示的,其实是肿瘤精心设计的防御三部曲。
首先,是城墙拒载导致的血管内皮失能。正常的血管内皮就像靠站的公交车,有粘附分子作为扶手让 T 细胞顺利下车。而肿瘤内皮把扶手全拆了,车门焊死,导致 T 细胞大军只能在血管里干流淌,完全无法渗出。
其次,是营地强拆引发的基质拓扑粉碎。进不去主城,T 细胞就在城外安营扎寨,形成相连的防御阵地。肿瘤立马派出由恶性成纤维细胞组成的拆迁队,像推土机一样把 T 细胞的营地硬生生推平、冲散,T 细胞沦为互不相通的孤岛,被长期消耗直至耗竭。
最后,是毒气室瘫痪造成的缺氧应激失能。极少数顽强的特种兵 T 细胞侥幸潜入了肿瘤核心,却遭遇了极度缺氧和 PGE2 构成的毒气室。在这种极端压力下,T 细胞内部蛋白质折叠崩溃,沦为丧失战斗力的应激态行尸走肉。
总而言之,免疫治疗无效,根本不是 T 细胞累了,而是被彻底的物理隔离和毒杀了。
纵观全篇,这绝对是一项极具视觉冲击力与机制深度的杰作。但在拍案叫绝之余,我们也必须保持严谨的学术审视。文章利用多维验证成功化解了样本量极小的尴尬,完美展示了单个患者体内惊人的空间异质性,但几把精密的解剖刀挖出的极致机制,若要升格为全人群的普遍定论,仍需更大规模真实世界队列的验证。同时,采用距离肿瘤较远的正常肝脏作为对照,也是在无法获取绝对健康人类离体活器官灌流模型下的最优妥协,毕竟前发性转移微环境往往在微转移早期就已经被重塑。此外,内皮屏障与缺氧失能并非全新的理论盲区,这篇预印本的划时代意义,更多在于它史无前例地利用亚细胞级空间组学,在人类离体活器官上为这些经典理论提供了最确凿的原位物理铁证。
瑕不掩瑜,牛津大学团队在 bioRxiv 上的这项工作,确立了一个颠覆性的空间药研范式:面对高度异质性的消化系统肿瘤肝转移,最锋利的武器不是无差别的细胞扩军,而是搞清楚微环境的空间拓扑逻辑。
通过空间定位与机制还原,该研究不仅为攻克 CRLM 补全了外堵、边耗、内杀的免疫逃逸三部曲,更引导整个行业重新审视联合用药战略。未来的破局点非常明确:一方面需要开城门,即逆转内皮失能,使用血管正常化药物让 T 细胞顺利渗出血管;另一方面需要清毒气,即改善缺氧应激,靶向 PGE2 等微环境毒素信号,防止进入肿瘤的 T 细胞发生不可逆的崩溃。
不破除物理屏障与代谢毒室,再好的免疫肿瘤药物也注定跨不过临床转化的死亡之谷。
Reference
1. Machine perfusion and single-cell spatial transcriptome mapping identifies novel immune escape mechanisms in colorectal cancer liver metastasis. bioRxiv. 2025
2. Proteotoxic stress response drives T cell exhaustion and immune evasion. Nature. 2025
注:本文图文解读基于公开学术文献,文中图表均引自原论文,仅供学术与行业交流。