Leica助力中国科大揭示光感知促进脑发育的神经机制
作者:史逸铭
婴幼儿大脑发育由先天基因(nature)和后天经验(nurture)的协同作用,其中后天接受的感觉刺激(包括视觉、听觉,触觉等)对促进大脑各区域之间神经突触连接的形成至关重要。视觉(光)作为人类最重要的感知能力,在出生后早期促进了多个大脑皮层的突触发育。然而,在发育早期视觉(光)是如何被感知、通过何种神经环路和分子机制促进了大脑发育、以及对婴幼儿成年后的认知学习能力的影响尚不明确。
哺乳动物的光感知起始于视网膜。视网膜中主要存在三类感光细胞:编码物体轮廓、运动和颜色等成像视觉信息的视杆细胞(rods)和视锥细胞(cones),以及介导非成像视觉功能(如昼夜节律光调节、瞳孔光反射和光调控情绪等)的视网膜自感光神经节细胞(intrinsically photosensitive retinal ganglion cells, ipRGCs)。在发育过程中,ipRGCs是最早具有感光功能的视网膜感光细胞,这提示ipRGCs可能是介导光促进幼年大脑发育的关键感光细胞。近日中国科学技术大学生命科学与医学部薛天教授、鲍进研究员团队揭示了ipRGCs的光感受促进哺乳动物幼年大脑发育的神经机制及对成年后学习能力从促进作用。相关研究成果以“Melanopsin retinal ganglion cells mediate light-promoted brain development”为题发表在国际著名期刊《CELL》上。
突触生成(synaptogenesis)是哺乳动物出生后大脑发育和神经突触连接的重要特征之一,其最显著的指标是神经元的自发微小兴奋性突触后电流(mEPSC)的频率和树突棘(spines)的数量。研究人员首先发现ipRGCs感光能力缺失的新生鼠,在出生后早期其多个感觉皮层及海马的椎体神经元mEPSC频率显著性降低;如果将ipRGCs感光能力正常的野生型新生鼠在出生后立即完全避光饲养,它们也出现同样的mEPSC频率降低的现象。同时,通过高尔基染色或单细胞电穿孔荧光标记方法描绘椎体神经元的形态(图1),研究人员发现缺失ipRGCs感光能力的新生鼠多个感觉皮层及海马的椎体神经元树突棘数量显著减少。这些结果说明ipRGCs的光感受在出生后早期介导了光促进大脑突触发生的现象。出生后在ipRGCs快速表达其感光蛋白melanopsin,可以显著提高ipRGCs感光能力缺失的新生鼠皮层和海马的突触生成,证明在发育早期,ipRGCs是介导小鼠早期光感受促进脑高级认知区域突触发生的充分且必要的条件(图2)。
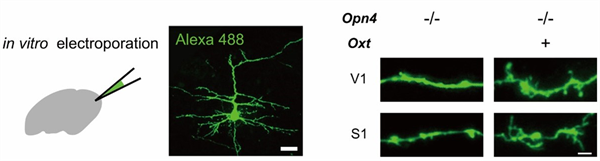
图1. 基于Leica SP8共聚焦扫描显微镜的单细胞电穿孔荧光标记实验

图2:发育早期ipRGCs介导的光感知通过激活视上核(SON)和室旁核(PVN)的催产素神经元,促进不同大脑高级认知区域(大脑皮层、海马等)神经元突触的协同发育。
进一步研究人员证明当ipRGCs被光激活后,会通过视网膜至下丘脑的ipRGCs - 视上核(SON) - 室旁核(PVN)神经环路,激活视上核和室旁核的催产素神经元,进而提升了脑脊液中的催产素浓度;而催产素作为神经元突触建立的关键调控分子之一,其浓度的提升促进了多个大脑皮层和海马的突触生成(图2)。通过离体脑片孵育催产素或出生后持续激活SON的催产素神经元,能促进ipRGCs感光能力缺失的新生鼠多个感觉皮层及海马的椎体神经元的突触生成,进一步证明了发育早期ipRGCs的光感受通过增加催产素的分泌而促进大脑发育。
发育早期ipRGCs光感受对大脑突触生成的促进作用,能显著提升小鼠成年后的学习能力。研究人员通过训练小鼠学习不同频率的声音刺激与奖励/惩罚的相关性,证明幼年期ipRGCs光感受的缺失,会导致小鼠成年后的学习速度显著下降(图3),而这种成年后学习能力的缺陷可以被出生后早期人为激活ipRGCs或视上核的催产素神经元所挽救。
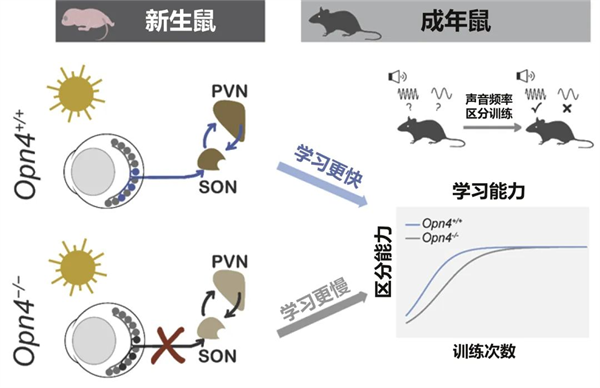
图3:发育早期ipRGCs介导的光感知提高成年后小鼠的学习能力。(示意图由中国科学技术大学人文与社会科学学院刘慧老师完善)
这项研究揭示了发育早期视觉(光)感知促进小鼠大脑高级认知区域神经元突触协同发育的感光、神经环路和分子机制,并揭示了发育早期光感知对成年脑高级认知能力的影响。该研究成果提示公共卫生研究应关注新生儿日常的光环境,同时也为开发有利于新生儿大脑认知发育的环境光照明设备提供一定的科学指导基础。
本研究中大部分荧光图片采集和所有神经元电穿孔荧光标记实验,均使用Leica SP8 共聚焦扫描显微镜(图4左)。离体电生理实验中的脑切片实验,均使用Leica vt1200 振动切片机(图4右)。

图4:Leica SP8共聚焦扫描显微镜和vt1200 振动切片机助力中国科大解析光感知促进脑发育的神经机制。左,Leica SP8共聚焦扫描显微镜。右,Leica vt1200 振动切片机。
中国科学技术大学生命科学与医学部博士生胡佳希、博士生史逸铭和鲍进特任研究员(现为中国科学院深圳先进技术研究院研究员)为本文的共同第一作者,中国科学技术大学生命科学与医学部教授薛天和中国科学技术大学生命科学与医学部特任研究员鲍进为本文的共同通讯作者。该成果得到了科技部、国家基金委、峰基金、安徽省、中科院以及中国科学技术大学的资助。
// 通讯作者

薛天:
中国科学技术大学生命科学与医学部教授
中国生理学会常务理事

鲍进:
中国科学技术大学生命科学与医学部特任研究员(现为中国科学院深圳先进技术研究院研究员)
论文链接:https://www.cell.com/cell/fulltext/S0092-8674(22)00912-6
Leica SP8已经被STELLARIS平台所替代,对相关产品感兴趣的老师们可以查看:
点击下图查看