徕卡共聚焦助力人脑类器官研究新突破——迷你大脑长眼睛了
新突破
当前,类器官研究如火如荼。这种在体外用3D培养技术对干细胞或器官祖细胞进行诱导分化形成的在结构和功能上都类似目标器官或组织的三维细胞复合体,包含多种细胞类型,突破了细胞间单纯的物理接触联系,形成了更加紧密的细胞间生物通信,细胞间相互影响、诱导、反馈,协作发育并形成具有功能的迷你器官或组织,能更好地模拟器官组织的发生过程及生理病理状态,因而在基础研究以及临床诊疗方面具有广阔的应用前景[1][2]。由诱导多能干细胞(iPSCs)产生的3D人脑类器官为研究大脑发育、疾病等提供了巨大的机会,这种脑组织体外三维培养系统是更好地理解发育性脑障碍发病机制的有力工具。由大脑类器官发育出各种不同的类脑区,组织形成离散区域,并能够相互影响,从而帮助我们了解脑组织细胞的多样性、复杂的相互作用和神经元网络[3]。
眼睛的发育是一个复杂的过程,了解它可为早期视网膜疾病治疗奠定基础。其中,研究视神经泡至关重要,因为视神经泡是眼睛的原基,其近端连接到前脑,为眼睛正常形成的关键环节。然而从多能细胞分化出来的离体视网膜类器官不能形成类似体内的视神经泡和视网膜上皮细胞层,这可能是因为离体视网膜类器官缺乏前脑(一种与视网膜发生发育相关的非视网膜类型组织[4])。
胚胎发育过程中,视泡由间脑通过器官发生多个阶段发育而来(图1A)。那么能否让大脑类器官像人胚胎发育般,组装产生两侧对称的视神经泡成为巨大挑战。利用iPSCs衍生的人脑类器官能否打破这个障碍?近期,杜塞尔多夫海因里希·海涅大学Jay Gopalakrishnan等人发表在 Cell Stem Cell上的一篇研究报道[5],成功让梦想照进现实。
快来看看作者是如何设计实验并借助哪些神器最终实现“迷你大脑长眼睛了……”
神助攻
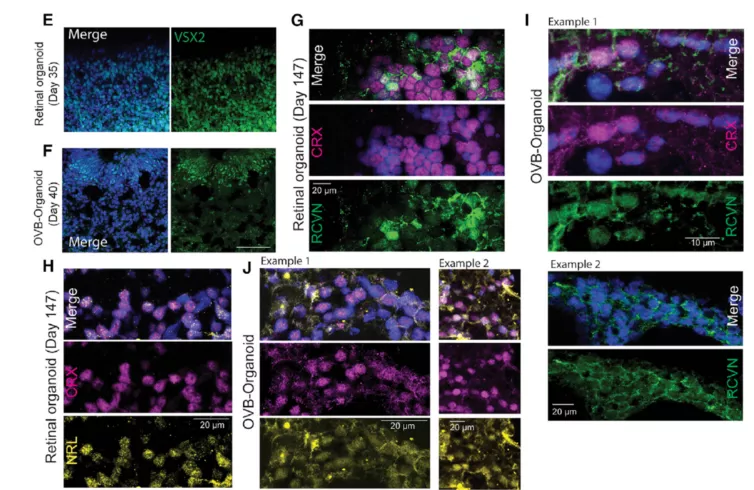
作者首先修改了多能干细胞诱导分化方案。从使用低密度的细胞数开始,并在神经外胚层扩张期加入0-120nM醋酸视黄醇。添加60nM的醋酸视黄醇可重复在第30天左右诱导产生色素结构(pigmented structures),并分布于大脑类器官的一极(图1B)。作者继续通过免疫荧光染色及使用徕卡共聚焦SP8多色荧光成像,研究色素结构区域的眼睛相关生物标志物。共聚焦图像显示该区域的RAX, Pax6和FOXG1免疫荧光信号呈阳性(图1C-D)。还观察到突出的SOX2阳性内陷区,显示VSX2和FOXG1梯度表达,表明类器官的视觉区域与前脑区分离(图1E-G)。并结合单细胞测序来进行细胞多样性的研究。
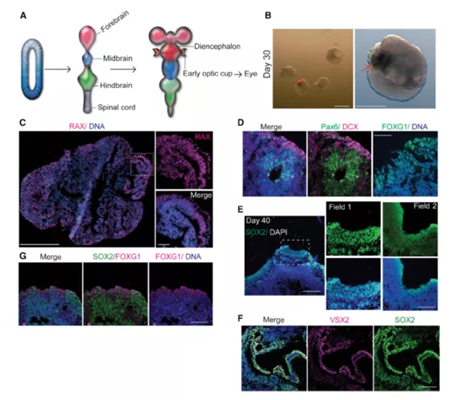
图1. 从iPSCs细胞生成人脑类器官及色素结构
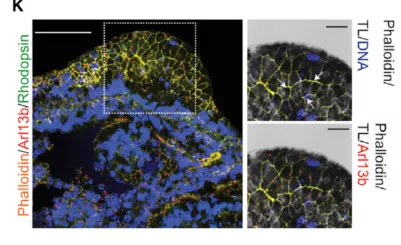
持续培养类器官,色素区域在50 ~ 60天内逐渐发育形成1 ~ 2个深色的视神经囊泡样结构,作者称这些器官为视泡脑类器官(OVB-organoids)。通过单细胞测序、转录组学比对及免疫荧光染色、徕卡共聚焦显微成像双重验证。发现OTX2阳性核在RPE细胞附近形成一层状结构,在更深的组织中也呈梯度表达。在一些情况下,OTX2阳性的细胞核,ONECUT2信号呈阳性,BRN3也呈阳性并显示出RGCs的层状结构(图2A-B-C)。并随后分析了早期视网膜发生的确定生物标志物,包括VSX2(神经视网膜祖细胞)、Recoverin、CRX和NRL,并以视网膜类器官进行对照。相比OVB类器官,视网膜类器官呈典型球形(图2D)。OVB-organoids中的观察结果在某种程度上与Capowski的1期和2期视网膜organoids中观察到的结果相似,这表明OVB-organoids包含有用于光受体发育的细胞。通过F-actin和Arl13b标记外层细胞膜和初生纤毛,共聚焦图像显示有组织的色素细胞呈现典型的蜂窝状形态,每个细胞都含有初生纤毛(图2K)。
然后作者研究了OVB类器官是否含有原始晶状体和角膜上皮样细胞等来自于表面外胚层的非神经元细胞类型。共聚焦图像显示位于每个视神经囊泡内的双侧aA/ ab -晶体蛋白阳性(图3A),这些结构被一层F -actin和Keratin-3阳性柱状上皮细胞包围,表明原始角膜上皮样层与晶状体样结构相邻(图3B)。超微结构观察到一个明显的圆形结构,可能是前房被原始细胞所包围角膜样上皮(图3C-D)。并在视神经泡附近发现了PCP4阳性,PCP4阳性细胞呈典型的体细胞形态,轴突延伸至100mm,穿透出视神经囊泡,从器官前部向后部迁移,表明阳性神经元可能已经从视泡迁移到更高阶的视觉区域(图3 E-F)。综上所述,作者成功设计出具有双侧对称视泡的大脑器官,并具有复杂产前眼发育的各种细胞类型(图3G)。
图2. OVB-organoid显示出发育中的神经视网膜
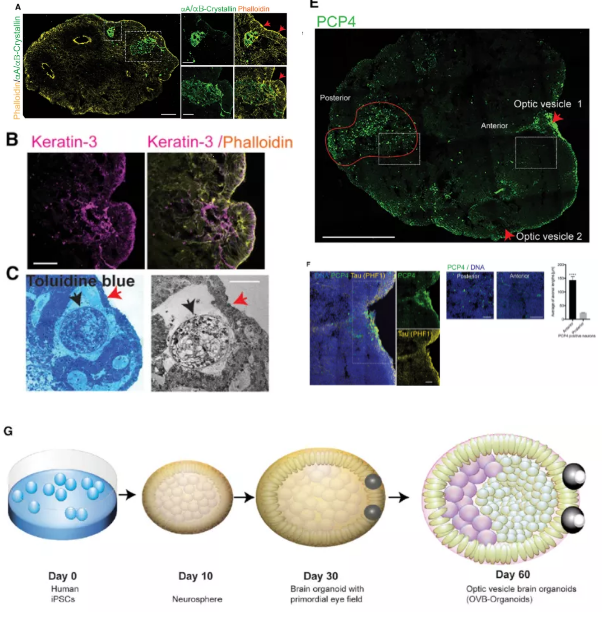
图3. OVB-organoid显示出非神经元成分
最后,作者结合转录组学数据,推断OVB类器官具有皮质神经元突触成熟特征并加以验证。共聚焦结果显示OVB表达Synapsin1阳性,成熟神经元标志物CTIP、髓鞘碱性蛋白(MBP)和层粘连蛋白等(图4A-B-C-D)。为了证实功能性神经元的存在,作者还进行了全细胞膜片钳记录,在OVB类器官的神经元细胞中可检测到明显的自发动作电位,并发现自发动作电位对豚毒素(TTX)有时敏感、有时抵抗,说明神经元细胞具有成熟功能,并设计光感实验做了进一步探索。
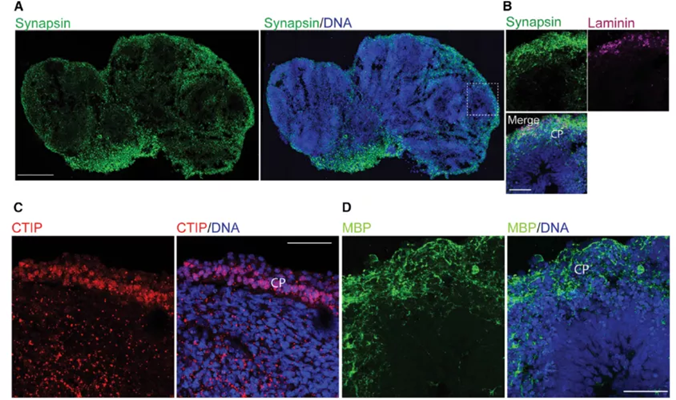
图4. OVB-organoid显示成熟神经元特征
期许未来
在这个人脑类器官的突破性研究当中,作者大量使用徕卡共聚焦系统获得出色的多色荧光图像,利用多种生物标志物来研究人脑类器官双侧视神经泡发育形成过程中多样的细胞类型。并结合单细胞测序、转录组学比对、超微电镜成像、全细胞膜片钳记录实验等手段,揭示这一过程与人眼胚胎发育的相似一致性,为使用同一类器官研究不同器官相互作用打开了新思路,同时为视网膜疾病机制和治疗的研究提供了新的强大工具。
朴朴实实的徕卡共聚焦使用案例,助力类器官研究领域新成就!
徕卡显微系统是有170多年悠久历史的显微设备专业制造厂商。如今新一代共聚焦STELLARIS正蓄势待发,期待与我们的新老客户合作,为生命科学各个领域的研究添砖加瓦、增加能量!
新一代STELLARIS共聚焦系统技能升级
杰出多色高清图像采集能力:
标配HyD S高灵敏检测器,检测范围覆盖410-850 nm,近红外成像一次搞定,多色能力轻松扩展。并且所有检测器自带双重制冷、光谱扫描、二代光子计数等高端检测器功能,帮助您看得更多。
- 标配Lightning超分辨模块,无需增加成本,让您轻松实现XY方向120nm、Z方向200nm的同时多色超高分辨率成像。
- 更有独家1nm步进连续可调超连续白激光技术。485nm-685nm或者440-790nm两款白激光任您选择。结合徕卡AOBS分光装置,精准、高效、温和的样品激发,更多信号,更自由的染料组合,更多维度激发光谱扫描,轻松拓展应用场景。
打开共聚焦成像新维度:
独门“技能”—TauSense:Leica STELLARIS突破性地将荧光寿命维度成像TauSense模块引入常规共聚焦成像平台。与传统共聚焦相比,STELLARIS激光共聚焦显微镜帮您获得多一个维度的样品图像,利用寿命信息来定性和半定量研究样品微环境改变、蛋白互作FRET实验,进一步扩展多色实验设计(基于荧光寿命),实时样品组分拆分及光谱串色拆分,帮助您发现更多。
以提升客户工作效率为使命:
标配ImageCompass智能一键式光路设置模块。保障客户高效、正确设置光路,一键智能优化采集参数,优化图像输出效果。从此您只需要关心您的实验本身,共聚焦操作交给ImageCompass轻松搞定。
- Navigator(导航式拼图)模块。无论是大样本全局、微观图像,还是多孔板、高通量、多焦点,Navigator统统帮您搞定。
- 共振扫描头+DSE(动态信号增强)+AiviaMotion的搭配,让您在STELLARIS上轻松追踪囊泡、血流、钙火花,保持速度的前提下获得高保真高信噪比的出色图像。