徕卡脑科学跨尺度成像——精细结构及功能成像
在脑科学研究的广阔领域中,对神经网络的精细结构与动态功能的深入理解是解开大脑奥秘的关键。然而,传统的成像技术往往面临分辨率不足的挑战,尤其是在密集神经追踪和分子亚细胞结构的精确定位上。这些限制极大地阻碍了我们对神经元连接、突触可塑性、以及细胞内蛋白互作等核心问题的深入探索。
为了克服这些障碍,我们推出了脑科学跨尺度成像解决方案,集成了共聚焦STELLARIS系统、高分辨模块Lightning、纳米超高分辨TauSTED Xtend,以及功能成像荧光寿命模块FALCON,为脑科学研究提供了优越的成像精度和功能分析能力。
共聚焦STELLARIS系统
作为徕卡脑科学成像方案的核心,STELLARIS系统以其卓越的光学性能和稳定性,成为研究神经元精细结构不可或缺的工具。该系统支持多通道同时成像,能够捕获到神经元网络中的复杂交互,特别适用于树突棘、轴突等细微结构的可视化。此外,STELLARIS系统还具备高度的灵活性和可扩展性,可根据具体研究需求配置不同的物镜和探测器,满足多样化的实验要求。
高分辨模块Lightning
针对更高分辨率的需求,徕卡的高分辨模块Lightning帮助研究人员能够更清晰地观察到神经元的亚细胞结构,如线粒体、内质网等细胞器,以及它们之间的空间定位关系。Lightning模块的应用极大地扩展了我们对神经元内部世界的认知边界。
纳米超高分辨TauSTED Xtend
为了进一步提升分辨率,徕卡发展了纳米超高分辨TauSTED Xtend技术。STED(受激发射损耗)实现了远超传统共聚焦显微镜的分辨率。TauSTED Xtend模块将这一技术推向了极致,使得分辨率达到纳米级别。这一技术革新使得研究人员能够直接观察到分子尺度的细节,如蛋白分子的精确定位和动态变化,为揭示神经元功能机制提供了强有力的支持。
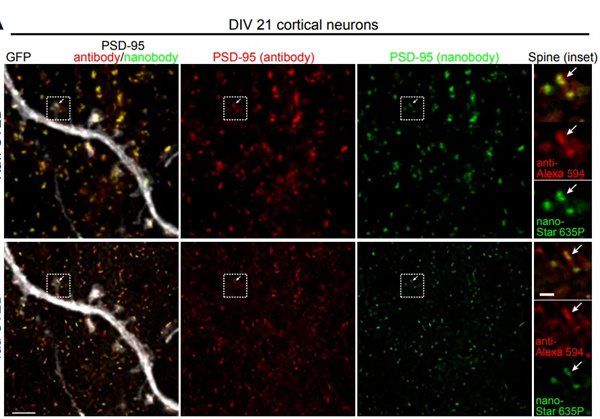
来自DIV21皮质神经元的GFP转染(灰色)树突的代表性Raw STED和Tau-STED图像[3]。用Alexa Fluor 594偶联二抗(红色)和直接与Abberior STAR 635P偶联的PSD-95纳米体(绿色)对培养物进行共染色。插图(方形)显示了PSD-95抗体和纳米体(箭头)共同标记的脊柱。Scale bars:2 µm; inset: 500 nm。
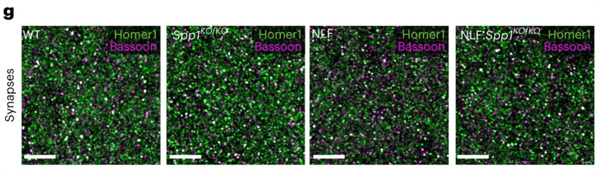
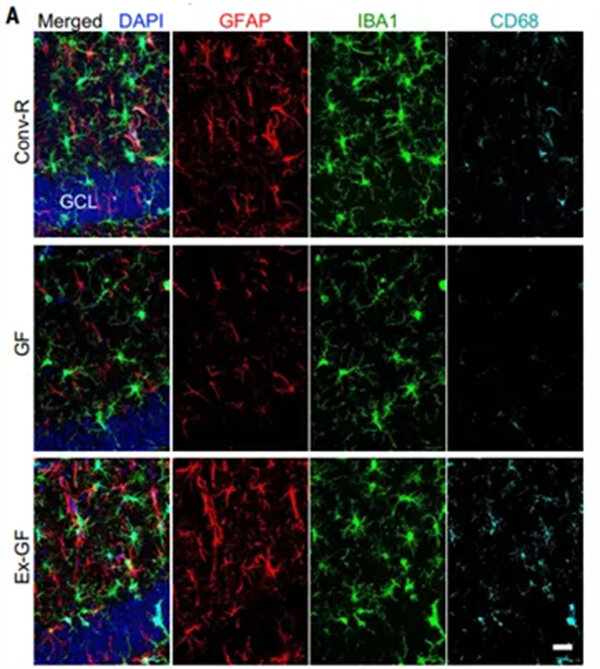
WT、Spp1KO/KO、AppNL-F和AppNL-F·Spp1KO/KO SLM中Homer1和Bassoon puncta共定位的STED图像[4]。Scale bars:5 µm。
功能成像荧光寿命模块FALCON
除了结构成像外,功能成像也是脑科学研究的重要方面。徕卡的功能成像荧光寿命模块FALCON通过测量荧光分子的寿命参数,提供了关于分子环境、相互作用以及动态变化的重要信息。这一技术特别适用于研究神经元活动时的蛋白构象变化、离子浓度波动等生理过程。FALCON模块的应用使得研究人员能够在细胞水平上实时观测神经元的功能状态,以及研究细胞内环境的变化,如氧化还原状态、pH值变化等,为深入理解大脑的工作原理提供了新的视角。
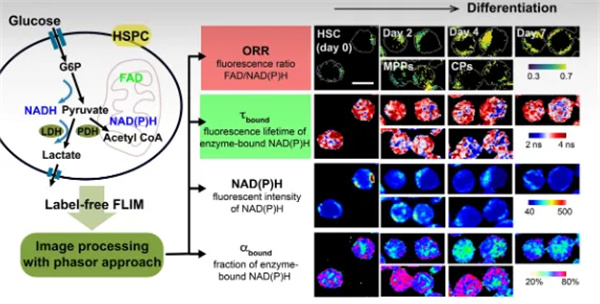
造血干细胞和祖细胞(HSPCs)代谢表型的FLIM分析示意图(左)和体外分化的造血干细胞和新分离的HSPCs沿分化层次的代表性图像(右)[5]。Scale bars:10 µm。
徕卡脑科学跨尺度成像解决方案,无论是精细结构的可视化还是功能状态的实时监测,这一方案都展现了强大的潜力和广泛的应用前景。随着技术的不断进步和完善,徕卡显微将继续为揭开大脑奥秘贡献更多的智慧和力量。
参考文献:
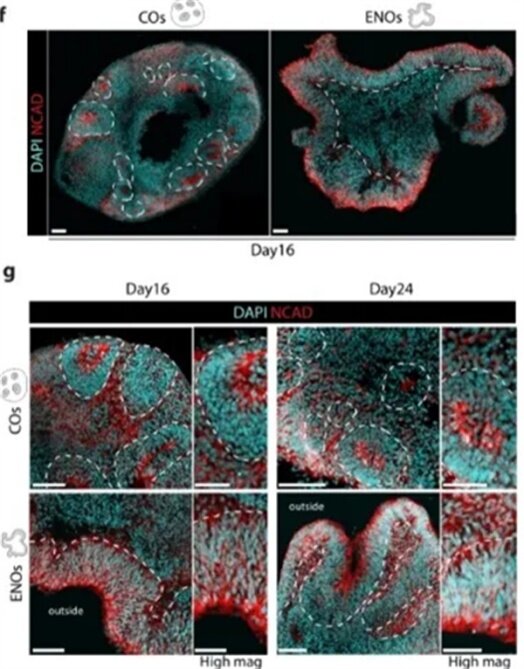
[1]Pagliaro, A., Finger, R., Zoutendijk, I. et al. Temporal morphogen gradient-driven neural induction shapes single expanded neuroepithelium brain organoids with enhanced cortical identity. Nat Commun 14, 7361 (2023). doi:10.1038/s41467-023-43141-1
[2] Dong-oh Seo et al. ,ApoE isoform– and microbiota-dependent progression of neurodegeneration in a mouse model of tauopathy.Science379,eadd1236(2023).DOI:10.1126/science.add1236
[3] Jones G, Akter Y, Shifflett V, Hruska M. Nanoscale analysis of functionally diverse glutamatergic synapses in the neocortex reveals input and layer-specific organization. Preprint. bioRxiv. 2024. doi:10.1101/2024.05.01.592008
[4] De Schepper, S., Ge, J.Z., Crowley, G. et al. Perivascular cells induce microglial phagocytic states and synaptic engulfment via SPP1 in mouse models of Alzheimer’s disease. Nat Neurosci. 26, 406–415 (2023). doi:10.1038/s41593-023-01257-z
[5] Hao Zhou et al. Label-free metabolic optical biomarkers track stem cell fate transition in real time. Sci. Adv.10, eadi 6770(2024). DOI:10.1126/sciadv.adi6770