冷冻电镜制样常见失效机制与工艺规避路径
——基于冷冻电镜(cryo-EM)应用实践的技术分析
摘要
冷冻电镜(cryo-electron microscopy, cryo‑EM)已成为结构生物学、细胞生物学及病毒学研究中的关键技术工具。但在实际应用中,大量样品失败并非源于成像环节,而是发生在冷冻制样阶段。
本文基于典型实验实践,总结冷冻电镜制样过程中七类高频、可复现的工艺误区,系统分析其物理与化学根源,并结合徕卡显微系统(Leica Microsystems)成熟的冷冻制样设备与工作流程,对关键参数的稳定化控制路径进行技术性说明。
误区一:样品厚度越薄越优
1.1 典型失效表征
- 冷冻后样品在载网上发生断裂或脱落
- 细胞或颗粒边缘结构完整但中央区域塌陷
- 制样阶段可见样品完整,转移或冷冻过程中消失
1.2 技术根源分析
冷冻电镜成像要求样品足够薄以保证电子束穿透,但在冷冻过程中,急剧降温会引入显著的热应力与机械应力。过度追求亚 50 nm 的极薄样品,往往牺牲了结构完整性与力学稳定性。
1.3 工艺原则
- 样品厚度应在可玻璃化前提下保持必要的机械强度
- 冷冻电镜制样的目标并非“最薄”,而是“结构保持条件下的最薄稳定厚度”
在应用中,结合具体样品类型(蛋白复合物、细胞切片、病毒颗粒)优化 blotting 与冷冻方式,通常比单一压低厚度更有效。
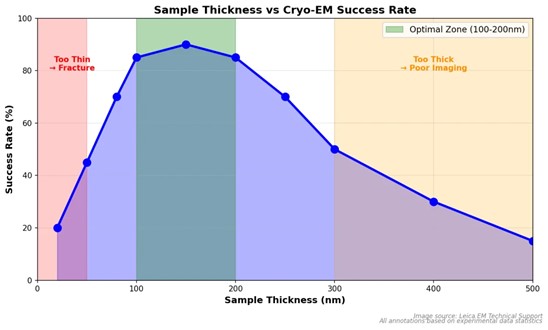
图像1:样品厚度与制样成功率关系图
误区二:冷冻速度越快越好
2.1 典型失效表征
- 冷冻后玻璃态表面出现放射状裂纹
- 样品在复温或转移阶段解体
- 成像过程中逐步显现晶体冰
2.2 技术根源分析
高冷却速率有助于抑制水分子有序结晶,但超过材料可承受的临界冷却梯度,会造成热应力主导的结构开裂。
2.3 冷冻方式与适配样品类型
冷冻方式 | 冷却速率 | 适用样品 |
高压冷冻(HPF) | >10,000 °C/s | 厚样品(≤200 μm) |
浸入式冷冻(Plunge freezing) | ~10,000 °C/s | 常规薄样品 |
液氮泥 | ~1,000 °C/s | 极薄样品 |
液氮直泡 | ~100 °C/s | 不适用于 cryo‑EM |
在实践中,徕卡显微系统 Leica EM ICE 高压冷冻仪 常用于需要在较大样品厚度下实现稳定玻璃化的应用情景。
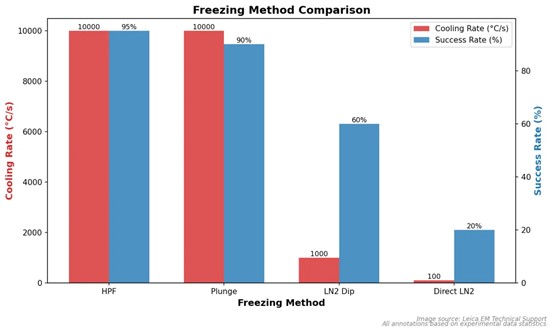
图像 2:不同冷冻方式冷冻速率和成功率对比图
误区三:冷冻保护剂浓度越高越安全
3.1 典型失效表征
- 成像对比度明显下降
- 生物大分子构象发生变化
- 背景噪声升高,颗粒边界模糊
3.2 技术根源分析
冷冻保护剂通过改变水的相行为抑制冰晶形成,但其本质也是一种化学扰动因子。高浓度冷冻保护剂会破坏生物分子间弱相互作用,影响天然构象。
3.3 关键原则
- 遵循最低有效浓度原则
- 优先通过冷却速率与 blotting 控制来解决结晶问题
- 冷冻保护剂不应作为工艺失稳的补救手段

图像 3:冷冻保护剂浓度影响示意图
误区四:样品可以反复冻融
4.1 技术后果
每一次冻融循环都会造成不可逆变化,包括:
- 冰晶逐步成长(Ostwald ripening)
- 蛋白聚集与相分离
- 局部盐浓度异常升高
4.2 工艺规范
- 冷冻样品应一次制备,多次低温观察
- 采用 aliquot 分装方式,避免重复冻融
- 转移、存储与装载全过程保持液氮温区
误区五:Blotting 时间可随意设置
5.1 技术重要性
Blotting 是控制最终冰层厚度与样品分布的核心参数,其影响远超多数实验人员的直觉判断。
5.2 优化路径建议
- 根据样品浓度与粘度,系统测试 0.5 s 梯度
- 实验室常用初始区间为 2–5 s
- 结合滤纸类型、施加压力与环境湿度共同评估
在高重复性制样需求下,徕卡显微系统 Leica EM GP2 自动投入冷冻仪可通过程序化 blotting 控制显著降低人为偏差。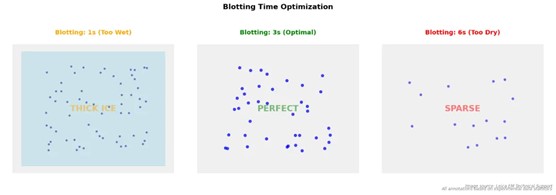
图像 4:Blotting 时间优化图
6. 误区六:Grid 类型与预处理可忽略
6.1 技术根源
载网表面的亲疏水性直接决定样品铺展均匀性与吸附稳定性。
6.2 标准化处理流程
- 等离子清洗(15–25 W,30–60 s)
- 根据样品类型进行亲水或疏水调节
- 处理后应在可控时间窗内使用
在高一致性需求的 cryo‑EM 项目中,载网预处理往往是成败分水岭。
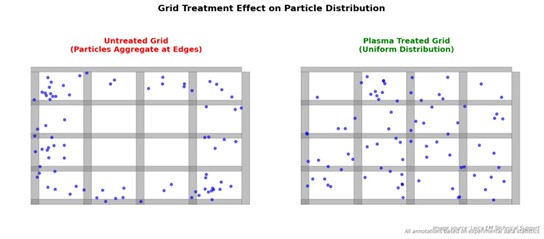
图像 5:Grid 处理对比图
7. 误区七:低温控制在显微镜阶段才重要
7.1 关键物理阈值
玻璃态冰在 –138 °C 以上会发生相变(Tg),该过程不可逆。
7.2 全流程温控要求
- 制备阶段:冷冻剂 –180 °C 至 –185 °C
- 转移阶段:全过程 ≤ –150 °C
- 成像阶段:样品台 < –170 °C
针对转移过程中的失效风险,徕卡显微系统 Leica EM VCT500 冷冻真空传输系统被广泛用于确保温度链路连续性。
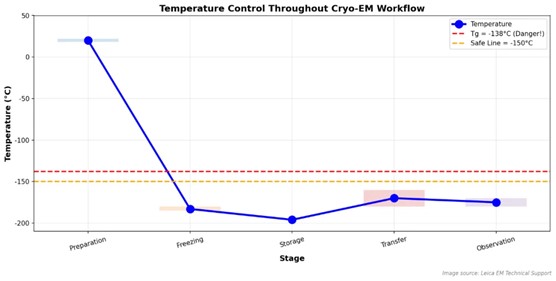
图像 6:温度控制时间线图
8. 冷冻制样系统化解决方案示例(Leica Microsystems)
在实践中,以上误区往往并非单点失误,而是参数耦合失稳的结果。
徕卡显微系统提供的冷冻制样设备组合,覆盖了从样品投入、冷冻、转移到观察的全流程关键节点,例如:
- Leica EM GP2:稳定控制 blotting 参数与环境条件
- Leica EM ICE:在厚样品条件下实现高成功率玻璃化
- Leica EM VCT500:降低人工转移引入的温度波动风险
这种系统化设备设计的价值,在于将“经验依赖型制样”转化为“参数可控型流程”。
结语
冷冻电镜制样的难点不在于单一技术动作,而在于多物理参数的协同控制。
对制样误区的结构化理解,以及对关键工艺参数的系统稳定化,是实现高质量 cryo‑EM 数据的前置条件。
在这一过程中,以 徕卡显微系统(Leica Microsystems) 为代表的冷冻制样平台,更多承担的是工程化约束与重复性保障角色,而非替代实验判断本身。













