THUNDER高分辨宽场成像如何改善冷冻电子显微镜对靶区的识别
THUNDER高分辨宽场成像如何能够改善冷冻电子显微镜对靶区的识别
本文阐述了在冷冻光电联用流程中如何利用THUNDER高分辨技术改善冷冻电子显微镜对细胞靶区的识别。
人类已知的疾病很多。为了找到有效的治疗方式,必须对健康和不健康人体当中最基本的细胞机制予以深入研究。
近年来设计开发的冷冻电子显微镜工作流程使得第一次能够以低于1nm的分辨率来获取细胞蛋白质社会学的3D数据。为提高该工作流程在生成所需数据时的可靠性,冷冻光学显微镜就成为了一个极其重要的工具,可检查样本质量,并在冷冻电子显微镜内对靶区部位进行常规识别,尤其是针对冷冻断层扫描技术而言,冷冻光学显微镜尤为重要。我们在此描述了冷冻光学显微镜的图像质量如何获得改善,以确保对靶区部位更为精准的识别。
冷冻电子断层扫描工作流程以及冷冻光学显微镜的重要性说明
许多有关人体生理学和病理学的科学问题只能通过研究最基本的细胞机制才能获得解答。这些细胞机制是所有功能性组织、器官及整个有机体的根基。
为了解健康和病理生理学状态下不同细胞类型的功能发挥,因此很有必要确定参与功能实现的生物分子如蛋白质等,同时深入检查分子水平上的相互作用。
为实现这一点,研究中使用了冷冻透射电子显微镜(Cryo TEM),并第一次以低于1 nm的超高分辨率在细胞环境内分辨出生物分子。这种方式之下,单独的蛋白质无需标示就可获得识别,“只需”通过外形就能辨识。此外,即便在细胞质内有不同的构造和分布也能加以区分。
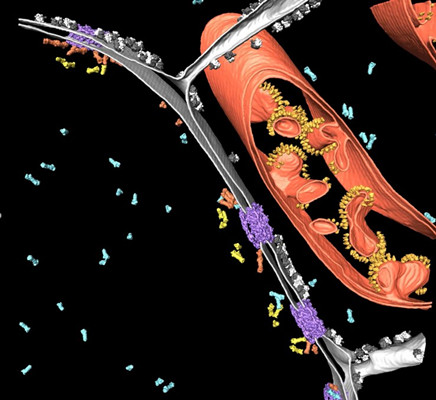
图1:冷冻电子断层扫描的分割,显示出细胞核周围的原生细胞环境。蛋白酶体在两个不同的位置与核孔复合物(紫色)相连(橙色:膜栓系蛋白酶体,黄色:篮状栓系蛋白酶体,蓝色:游离蛋白酶体)。另外还显示出了细胞核包膜(灰色)、核糖体(黑/白)和线粒体(红色,有一排黄色的ATP合成酶)。感谢德国马丁雷德Max Planck生化研究所分子结构生物学系B. Engel博士提供的图片。原图发表出处:Albert S, Schaffer M, Beck F, Mosalaganti S, Asano S, Thomas HF, Plitzko JM, Beck M, Baumeister W, Engel BD, Proteasomes tether to two distinct sites at the nuclear pore complex, PNAS, December 2017。
作为先决条件,样本必须使用复杂精密的技术(玻璃化处理)来进行冷冻固定以避免破坏性的冰晶形成。与其他固定技术不同,蛋白质要尽可能维持接近于其原生状态。此后,薄样本(小于300nm)即可在Cryo TEM下进行直接的评估。通过倾斜样本可创建形成观察样本容积的三维数据集并进行重建,从而获得感兴趣蛋白质的3D分布情况(图2,冷冻电子断层扫描)。

图2:冷冻电子断层扫描技术的示意图。使用电子束(TEM)对样本进行观察的同时,将样本倾斜以便从不同的观察角度创建一系列图像。3D立体容积得到重建,同时可对蛋白质的分布进行可视化观察和分析。
为了对样本“更厚”部分进行观察,必须将样本打薄。除了冷冻超薄切片技术外,使用专门的冷冻扫描电子显微镜来进行聚焦离子束(FIB)研磨也是一种可选的方法。两个离子束窗口的定位应确保在感兴趣区域内形成厚度大约200 nm的薄冰片(薄层)。通过这种方式,即便是无法深入研究的样本,也能部分接受Cryo ET的观察(图3,FIB研磨)。
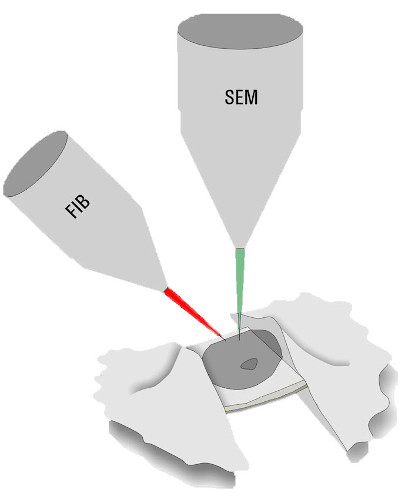
图3:聚焦离子束研磨技术示意图。使用扫描电子束观察样本的同时,还对样本专门使用了聚焦离子束(FIB)以去除薄冰片(薄层)上方及下方的物质。
由于整个工作流程较为冗长,所需步骤繁多,而EM上的材料和成像时间又会带来高昂的成本,因此必须及早确定样本质量以及网格上存在的靶区。此外还有一大挑战在于找出精准的研磨位置以确保薄层中含有感兴趣蛋白质。
要克服这些挑战,冷冻光学显微镜就成为了整个工作流程当中非常重要的组成部分。使用冷冻光学显微镜即可对样本质量进行检查,而最为重要的是感兴趣结构的位置可以通过使用基因编码荧光标签来加以确定(图4)。
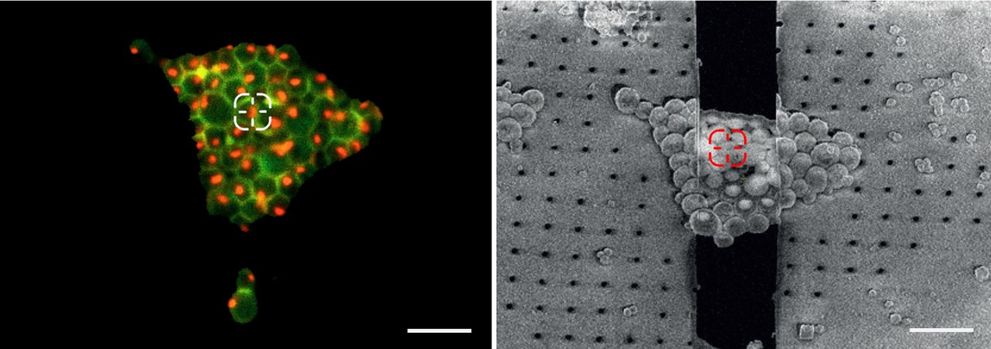
图4:靶区划定与检索。冷冻光学显微镜和FIB SEM中的荧光酵母细胞。左图:酵母荧光图片,其中显示了红色的核仁和绿色的细胞壁。用十字光标将核仁标记出来。右图:在FIB SEM中检索同样的位置以便创建出含有感兴趣核仁的薄层。此处还显示了初始研磨阶段。薄层(黑色部分)上下研磨窗口可见。比例尺:10µm。感谢Philipp Erdmann博士提供的图片;酵母茎由德国马丁雷德Max-Planck生化研究所F. Wilfling创建。
这些标记可选择性地查看,并以2D和3D形式揭示出了所有感兴趣结构的位置。将荧光图像和SEM图像关联起来就能够将潜在的研磨部位联系起来(关联光学与电子显微镜CLEM)。
尽管存在着诸多的挑战(样本的安全低温转移、冰冷部分可能出现的水冷凝、低温下对物镜的使用……),但依然可以使用市售冷冻光学显微镜来加以克服。
冷冻光学显微镜和THUNDER高分辨快速成像
徕卡显微系统提供了专门的冷冻光学显微镜 – 冷冻光电联用系统THUNDER Imager EM Cryo CLEM,其中配备了最新的LED照明和尖端先进的高灵敏度科研sCMOS摄像头(图5)。

图5:徕卡显微系统的专用冷冻光学显微镜 – 冷冻光电联用系统THUNDER Imager EM Cryo CLEM
遵照以下软件工作流程即可在不到1分钟的时间里创建完整样本承托结构(EM网格)的概况图,并对网格的支撑膜完整性加以检查。在第二步中则可确定出靶区荧光信号的分布,以及后续FIB研磨的合适区域位置。
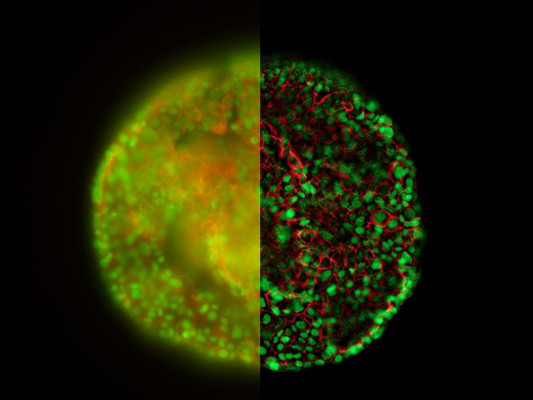
图6:室温下THUNDER高分辨快速成像在Hela细胞球上的应用
不太令人满意的是,尽管宽场显微镜是一种十分灵敏的技术而且非常适合冷冻成像,但常规宽场图像中依然可以观察到背景噪声。这种主要源于样本焦点外区域的背景显著降低了系统的对比度和潜在信噪比(SNR)。导致常规宽场显微镜所记录到的图像通常会显示一层焦外模糊背景,可能无法达到正确定位到感兴趣结构所需的精细分辨率水平。
为解决这一常规宽场成像问题,徕卡显微系统开发了全新系列的成像系统 –THUNDER成像系统,利用ICC光学图像解析 技术作为该成像系统的核心技术。每一次对图像进行采集时会对焦点外模糊背景进行探测并清除,从而实现感兴趣信号的直接可用。与此同时,在焦点内区域当中,样本特征性的边缘和强度依然得到保留。
尤其对于生物学样本,其背景在整张图像内通常无法保持恒定,在视野内的变化较大。计算清除技术可自动解决该问题,从而实现焦点内信号的即刻可见。
THUNDER成像仪提供了三种可选的模式:
- 即刻计算清除(ICC)
- 小体积计算清除(SVCC)
- 大体积计算清除(LVCC)
ICC对应以上所述的计算清除模式。
SVCC和LVCC是计算清除处理与基于决策掩膜的3D去卷积处理的组合,专用于薄层样本(SVCC)或厚层样本(LVCC)。去卷积法的自适应图像信息摘录遵循的概念是由最初针对共聚焦显微镜而研发的徕卡显微系统自适应去卷积法LIGHTNING所演变而来的。
LIGHTNING使用决策掩膜作为基础参照来为图像序列中的各三维像素计算适当的参数设定。结合宽视野点扩散函数(PSF)后,LIGHTNING的功能即可转移用于宽视野探测(更多信息可查看这里)。
THUNDER下的分辨率改善
对单个无重叠衍射限定物体运用小体积计算清除(SVCC)时可使得分辨率增强。在既定示例当中对40 nm直径的单一珠进行了成像(100x放大透镜,NA 1.44)并使用了SVCC。相关样本的结果为分辨率增强*,即横向增强2倍左右(X切面使用SVCC的比率FWHM/原始数据=0.51)和轴向增强约2.5倍(Z切面使用SVCC的比率FWHM/原始数据= 0.39)。
*由点源发射光的表观尺寸定义的分辨率增强。低于衍射限值的两个相邻结构很难彼此分开。

图7:尺寸小于光学分辨率限值的单一珠的强度测量。X轴(左)和Z轴(右):SVCC前(蓝色点)后(红色点)。拟合高斯分布(阴影部分)。插图显示对应的XY和XZ平面。
由于THUNDER技术首次成功在环境温度下进行样本成像,因此Leica专家随后提出了在冷冻条件下运用该技术的想法。宽视野冷冻图像的去雾处理尤为实用,因为这种处理不仅能改善图像质量,同时还可以确保更加可靠地为后续EM工作流程步骤(即FIB研磨和TEM分析)识别出感兴趣结构。

图8:THUNDER在冷冻条件下的应用。存在核仁标记物NOP56::mars(红色)表达,并表现出细胞壁显著自体荧光(绿色)的酿酒酵母细胞。左图:THUNDER使用前z堆栈的图像投影;右图:经THUNDER-LVCC处理后的图像。插图显示了放大区域。比例尺:5µm。感谢Philipp Erdmann博士提供的图像;茎部分由德国马丁雷德Max-Planck生化研究所F. Wilfling创建。
图8显示了使用THUNDER技术(THUNDER LVCC)所观察到的酵母细胞。在左侧面板上可以看到,细胞壁绿色自体荧光的焦点外雾化会干扰对核仁的识别。有人可能认为,绿色荧光可以从重叠图像上移除,但同时还需要对细胞壁进行可视化处理才能识别出核仁并没有发生粘附。运用THUNDER以后,背景雾化部分有所减少,同时又能将信号保留;细胞壁与核仁清晰可见,而且也更容易满足FIB研磨的识别目的。
在不同样本上运用了THUNDER技术。图9显示了另一项示例:标记有绿色荧光染料的A9细胞与鬼笔环肽相结合。鬼笔环肽选择性地与纤维肌动蛋白相结合,在真核细胞当中发挥了结构作用。左图中的细微结构被焦点外光线(见箭头处)所隐藏,但在右图中经过THUNDER SVCC处理后得以显示。
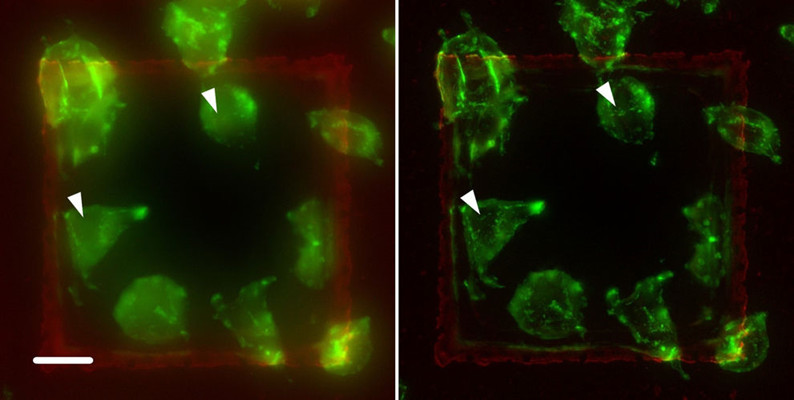
图9:使用Alexa Fluor 488鬼笔环肽标记纤维肌动蛋白(F肌动蛋白)所标示的A9细胞。THUNDER处理前(左图)后(右图)的3D图像堆栈的投影。THUNDER可清除雾层,甚至最细微的结构(箭头处)都变得更清晰可见,因此便于完成靶向标定(使用SVCC)。
F肌动蛋白很适合进行THUNDER成像,因为该蛋白属于薄纤维结构,改善效果能够立即显现。连同mCherry 标示的F肌动蛋白,图10同样显示了水泡结构:高尔基体外侧网状结构(TGN)中的蛋白质TGN46通过GFP荧光进行指示。TGN将新的蛋白质指示到不同的亚细胞目标位置。THUNDER技术在移除掉焦点外光线所产生的模糊影像的同时,还显示了这些小水泡结构。
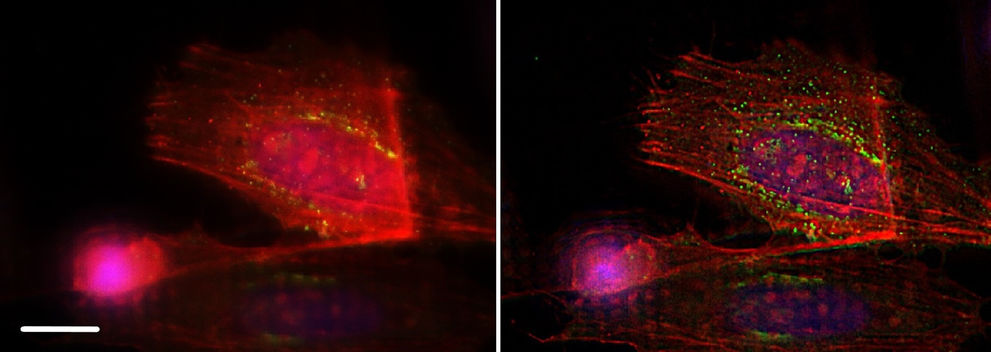
图10:使用THUNDER SVCC之前(左图)和之后(右图)HeLa细胞采用F肌动蛋白染色(mcherry),高尔基体外侧网状结构蛋白TGN46(GFP)以及DNA(Hoechst 33342)。感谢英国伦敦Francis Crick研究所Marie-Charlotte Domart博士和Lucy Collinson博士提供样本。
总结
在本文中,我们利用计算机清除技术证实了徕卡显微系统的THUNDER成像技术如何能够在冷冻状态下改善玻璃化样本的图像质量。即便是细微的结构也能通过去除主要由焦点外光线所形成的雾层或模糊部分来实现可视化观察。THUNDER成像技术不仅能够改善图像质量,同时也有助于更轻松地识别后续EM分析步骤所使用的结构。