如何为免疫荧光显微镜制备样本
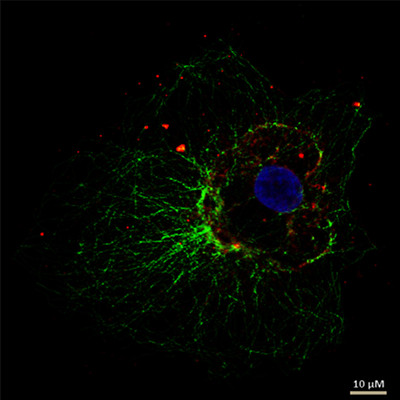
免疫荧光(IF)是一种用于可视化观察细胞内过程、状态和结构的强大工具。 IF制剂可通过多种显微镜技术(如激光共聚焦、宽场荧光、全内反射成像、基态淬灭显微成像等)来加以分析,具体取决于应用目的或研究人员的关注重点。 与此同时,在很多使用至少一套简易荧光显微镜的研究工作组当中,IF早已成为不可缺少的一部分。
IF实验的核心部分是两种不同组分的组合:
首先是特异性抗体,用于形成免疫复合物来标记细胞内需要研究的分子,大多数情况下为蛋白质。
- 其次是荧光色素,与免疫复合物耦合,因此可以用显微镜观察目标结构。

图 1: 图中显示了间接免疫荧光的典型工作流程,上皮细胞粘附在盖玻片上生长。 培养后细胞被固定,因此用化学交联剂(如甲醛)将其杀死。 再用清洁剂进行透化处理,使抗体穿过细胞膜。 用正常血清、奶粉或牛血清白蛋白来进行封闭,可减少抗体与非靶向结构的非特异性结合,从而减少假阳性信号。 接下来与一抗进行孵育,特异性识别靶向分子上的表位。 在第二个培育步骤中,应用荧光耦合二抗,与一抗结合来实现靶向结构的可视化观察。 抗体孵育后,用DAPI或Hoechst等嵌入DNA的染料进行细胞核染色。 使用封固介质(例如Mowiol或Prolong Gold)将盖玻片封固在载玻片上后,IF即已准备好进行显微镜观察。
直接与间接免疫荧光
根据实验类型的不同,有两种不同的IF变体可以使用: 第一种是直接IF或一级IF,一种具有特异性的一抗,能够与荧光色素连接,用于结合靶向结构并实现直接可视化观察。
第二种变体是间接或二级IF,这种变体需要采用两步式培育。 首先,特异性一抗识别靶向结构。 然后应用与一抗特异结合的荧光色素耦合二抗。
这种特异性是通过引导二抗抵御产生一抗的物种而获得的(见抗体和荧光色素章节)。 比较两种IF变体可见两者各有不同的优缺点:
通过耦合一抗和荧光色素,耗时的清洗和培育步骤被省略,所以直接IF比间接IF更快。 因此,直接IF更易于处理,适合于在标准IF实验中(例如在临床实践中)对样本进行快速分析。 但必须使用一种功能良好且对其抗原高度敏感的一抗。 这同时也是一个缺点,因为荧光耦合和验证的一抗成本较为高昂。 此外,每个靶向结构都需要一个单独的一抗,与间接IF相比,抗体与直接IF中的荧光色素的连接会限制实验设计的灵活性。
这种灵活性是间接IF的显著优势之一。 通常在IF反应过程中,同一样本都会有几个不同的靶结构需要实现可视化观察,因此必须为每个靶向分子选择一个离散的荧光色素。 在间接IF中,不同的荧光耦合二抗可以与不同的一抗结合(当然还要考虑到物种的反应性)。 相较之下,如果想在直接IF中对靶向结构“玩”颜色组合,则需要为每一种颜色使用单独的一抗。 间接荧光的另一个优点是二抗的信号放大。 多个二抗分子可与一个一抗结合来实现荧光增强,这意味可减少使用一抗。
间接IF的工作流程可能需要花费更多时间,但由于一抗和二抗能够组合而且整个操作过程的经济性更高,因此间接荧光成为了绝大多数研究人员的首选方法。
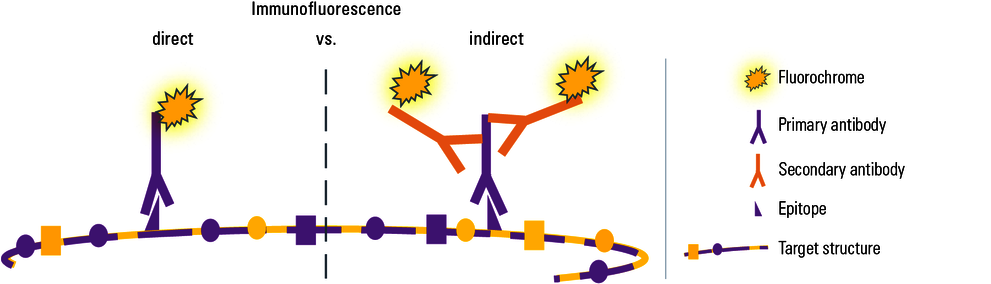
图 2: 有两种方法通过免疫荧光显示靶向结构: 在两种变体中,一种特异的一抗用于识别靶分子上的特定表位。 在此图中,靶分子由几个相同的蛋白质亚单位(=大分子)组成,因此会在每个亚单位上表现出几个相同类型的表位。 为方便简化,此处只描绘了一个表位。
直接IF中,一抗直接连接到荧光色素,在显微镜下观察靶向结构。
间接IF中,荧光耦合二抗在第二培育步骤中使用,从而专门对一抗进行标记。 因为多个二抗分子可以结合到一个一抗上,所以选择抗体和荧光色素的灵活性更大,并能够进一步放大信号。
抗体和荧光色素
高质量的IF染色当中,最重要的工具是良好的一抗。 同时,几乎每种细胞类型中的每种蛋白质都有一种或几种市售抗体。 但此处需要强调若干重要注意事项。
要根据IF染色来做出精确的科学或临床声明,就必须确保一抗对其目标抗原的特异性。 在操作中,研究人员不应完全依赖商业供应商的说明。 应根据之前的使用经验以及文献中确认有效的一抗来进行抗体选择。 查看制造商网站上的抗体数据表,查看IF染色的可用图片并与自身期望相比较,或者与其他已发布的插图进行比较。 注意抗体的克隆性,因为单克隆抗体只与一个表位特异性结合,而多克隆抗体可识别多个表位,因此更有可能存在非靶向结构的非特异性标记。 所以,特异性较高且性能较优的单克隆抗体通常更昂贵,但也能获得更好的效果。
如希望开展多色间接IF实验,则不同的一抗必须衍生自不同的物种,以便在之后通过荧光耦合二抗来区分免疫复合体(见表1)。 比如,您希望使用小鼠衍生的抗体抗蛋白A、兔衍生的抗体抗蛋白B和大鼠衍生的抗体抗蛋白C来实施IF检查。 在选择二抗时必须记住,每种抗体都只能特定识别一种一抗。 此外,在这三种二抗的例子中,荧光色素的波长光谱必须不同,以便在显微镜分析中辨别荧光信号。 如今,可以买到与荧光色素相连的二抗,其波长范围从紫外线到红外线,几乎可以针对任何物种的一抗。 因此,研究人员目前仅受到现有显微镜(滤光片组、激发激光器)配置的限制。
| 靶蛋白 | 蛋白质 A | 蛋白质 B | 蛋白质 C |
|---|---|---|---|
| 靶向物种 | 人类 | 人类 | 人类 |
| 一抗 | 抗蛋白 A | 抗蛋白 B | 抗蛋白 C |
| 一抗物种反应性 | 小鼠抗-人 | 兔抗-人 | 大鼠抗-人 |
| 二抗物种反应性 | 羊抗-小鼠 | 羊抗-兔 | 羊抗-大鼠 |
| 荧光素激发/发射光谱 | 490/525 纳米 | 556/573 纳米 | 650/665 纳米 |
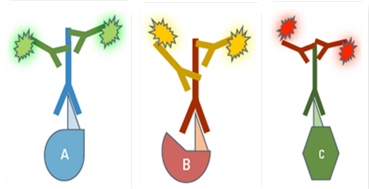
表 1:此处的多色间接IF示例演示了如何在同一个细胞中同时标记三种不同的蛋白质。
三种蛋白质的一抗必须来自不同的物种,以便用三种不同的荧光色素耦合二抗来进行检测。 二抗的荧光色素必须在波长光谱上有所区分才能在显微镜下进行不同的分析。 对示例图像中描绘的细胞还使用Hoechst 33342进行处理,完成了细胞核染色。 在Leica TCS SP2上进行显微镜检查。
样本
IF方案存在于多种不同的样本当中。 最简单最常用的方法是对细胞培养物中的培养(真核)细胞进行染色。 贴壁生长的细胞可以接种在盖玻片上,采用多微孔插入或者直接接种在玻璃底培养皿上并在所需的时间用于IF检查。 IF还可在细胞涂抹于载玻片(例如细胞离心涂片)后用于悬浮细胞的检查。 在这两种情况下,需重点分析细胞内的过程或结构,这被称为免疫细胞化学(ICC)。
另一方面,在免疫组织化学
(IHC)typo3/中,通过组织特定的环境联系来检查是否存在蛋白质或分子。 此处器官制备的超薄切片(通常包埋在石蜡中)用于比较研究健康器官与疾病器官中蛋白质的表达。 除了制备组织切片外,还可以对整个生物体进行IF检查,这一过程被称为“整体IHC”。 为此可使用不同模式生物的胚胎如小鼠、鸡或斑马鱼等,或植物模式生物如拟南芥。 在整体IHC中会受到样本尺寸和相关IF试剂透化深度的限制。 单独的孵育步骤比培养细胞的染色要长。 此外还必须提供带有特殊光学设备的显微镜用于大样本分析。
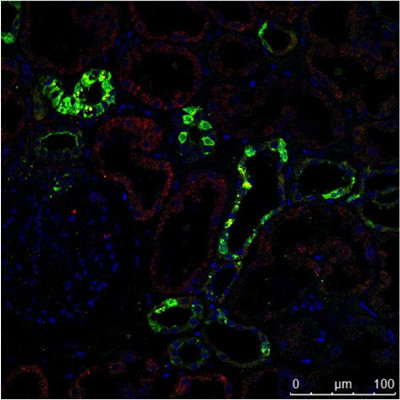
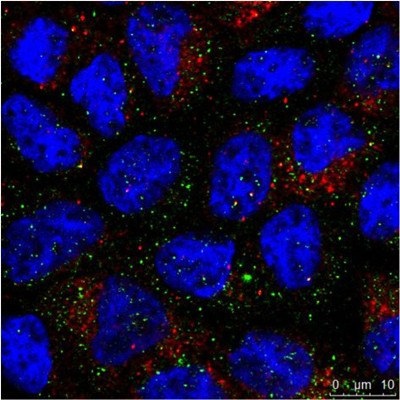
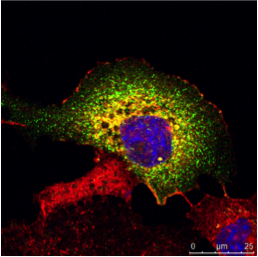
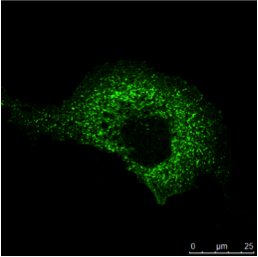
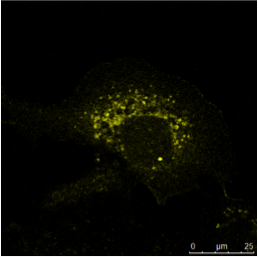
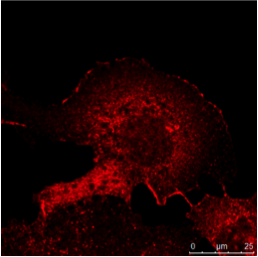
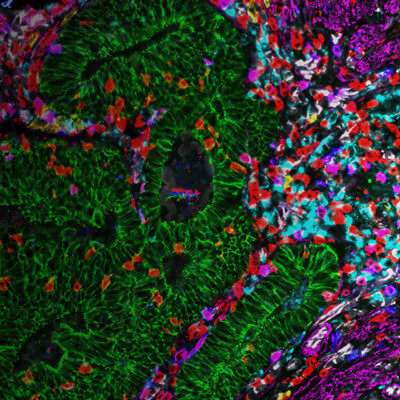
图3:a) 人类肾脏的免疫组织化学(IHC)染色在不同的结构中显示了不同的细胞类型(如肾小球、近曲小管、远曲小管)。
绿色荧光色素标记蛋白的表达仅限于特定的细胞类型,而红色标记蛋白则广泛表达。 b) 免疫细胞化学(ICC)图像显示间接免疫荧光对同一类型细胞(MDCK)中的两种蛋白质的染色情况。
此处无法开展组织特异性研究,但是如果两种蛋白质在同一个结构中共定位则可以进行分析。 对两个样本使用Hoechst 33342进行处理,完成了细胞核染色。 在Leica TCS SP2上进行显微镜检查。
清洗步骤
在IF程序中应特别注意清洗步骤,因为适当的清洗可以提高IF质量。 PBS是一种标准的清洗缓冲液,而PBS++或PBS-T等变体也很普遍。 PBS++含有1 mM CaCl2和MgCl2,推测其具有防止细胞分离的膜稳定作用。 对于PBS-T,添加最终浓度为0.05%的清洁剂Tween 20,目的是增加抗体的结合特异性。 请务必注意小心地涂抹并吸取清洗缓冲液以免细胞从培养容器或盖玻片上脱落。
如有足够的时间,请在吸取缓冲液时等待几分钟,以确保清洗缓冲液有效扩散到样本中。 IF程序的各个清洗步骤在下面的标准方案中列出。
传统IF反应的各步骤描述如下。 本文结尾附有最常用的间接IF与培养细胞的标准程序。
固定
固定是IF程序的第一步。
其目的是保持细胞、细胞结构或组织处于其当前状态,并通过化学试剂长期保存。 在固定过程中,重要的是细胞结构尽可能保持其原有的构象。 不同的固定方法对IF有用,每种试剂对一抗表位有不同的影响。 抗体结合位点可能被掩盖或被固定所破坏,这会损害IF染色质量。 由于每种抗体以不同的方式与抗原结合依赖于不同的固定化合物,因此有必要尝试新抗体的几种固定方法。
通常,合适的固定剂规格可以在抗体的数据表上找到。 理想的固定应能够保存细胞和亚细胞结构,并为良好的抗体结合暴露出抗原。 实际上,您必须在两者之间取得平衡。
固定试剂可以大致划分成2组:化学交联剂和有机溶剂。
化学交联剂如通过游离氨基形成的福尔马林交联蛋白;细胞形态在大多数情况下保存良好。 但抗原也可能发生交联,进而可能减少抗体结合。 戊二醛对细胞结构也有保存固定作用,但会导致显微镜下观察到样本有很强的自发荧光(见对照章节)。
有机溶剂如甲醇或丙酮等具有脱氢作用并沉淀蛋白质,从而将其固定在细胞环境中。 但切记,在该过程中可溶性分子和许多脂质成分都会丢失。
| 固定 | 效应 | 优点 | 缺点 | |
| 化学交联剂 | 甲醛 | 通过游离氨基形成的交联蛋白 | 细胞形态保存良好。 有利于已存在的荧光蛋白。 | 抗原同样有可能发生 |
| 戊二醛 | 细胞形态保存良好。 有利于已存在的荧光蛋白。 | 抗原同样有可能发生交联 强自发荧光 | ||
| 有机溶剂 | 甲醇 | 脱氢和蛋白质沉淀固定。 细胞将同时透化。 | 细胞结构保存良好。 与化学交联剂相比程序更快。 | 对许多表位有强烈的负面影响。 不适用于荧光蛋白。 可溶性组分和脂质组分 |
| 丙酮 | 减少对表位的破坏。 程序操作更快 | 不适用于荧光蛋白。 可溶性组分和脂质组 |
表 2: 固定试剂。
透化
通过透化处理,抗体可以进入细胞内结构,否则抗体就无法通过细胞的脂膜。 根据固定类型,有时需要单独的透化处理。 用有机溶剂固定时,细胞膜已经具有渗透性,您可以直接进入封闭步骤。 用化学交联剂固定的细胞需要用清洁剂进行额外处理以实现透化。 使用Triton X-100或NP-40等传统清洁剂,但也可使用皂甙、Tween 20或洋地黄皂甙。 同样,根据应用的物质、浓度和培养时间会得到不同的结果,因此实验人员应该在开始时尝试不同的参数。 典型的步骤是在室温下用0.1% Triton X-100在PBS中透化15-20分钟。
如果希望通过IF来分析脂质相关蛋白或膜蛋白,则应谨慎开展透化步骤(=脂质去除)。 比较理想的选择是皂甙,能选择性去除质膜上的胆固醇,使细胞内的膜基本上完好无损。 如果在抗体染色前忽略了透化处理(只能通过化学交联剂固定),则可以专门标记细胞外质膜结合抗原,以便将其与胞内抗原分开来。 核酸染料如DAPI或Hoechst(见细胞核染色和样本封固章节)具有膜渗透性,因此不需要透化处理。
封闭
封闭是在细胞内最大限度降低一抗非特异性结合的重要步骤。 为了实现这一点,可以使用来自牛血清白蛋白(BSA)、奶粉或血清中的蛋白质。 关键在于,这些封闭蛋白质并不源于产生一抗的物种,否则二抗对于一抗的特异性就会损失。 如果您使用的是二抗,如山羊产生的抗小鼠一抗,则理想的封闭试剂是正常的山羊血清。 通常使用浓度为1%(奶粉,BSA)至5%(正常血清)的封闭溶液,并在清洗缓冲液中稀释。 在室温下孵育30-60分钟。
免疫反应
经固定、透化和封闭步骤制备样本后,会开始进行免疫反应。 样本现在与特定的一抗一起孵育,以标记所需的靶结构。 几种一抗可同时应用于样本。 如上所述,在间接多色IF中,几种一抗必须来源于不同的物种。 首先根据制造商的要求,在选定的封闭溶液中进行抗体稀释。 如果对染色不满意,或者如果制造商没有提供任何关于有效稀释的信息,您应该尝试使浓度保持在1:50到1:1000之间。 根据抗体的亲和力,孵育时间可能会有所不同。 默认培育时间为室温下1-2小时;也可以在4℃下过夜。
如果选择直接IF,则可在一抗孵育后直接进行封片,因为一抗已经带有荧光色素。 在间接IF当中,二抗现在已经对一抗进行了荧光标记。 这里的关键点在于使用一抗孵育后要充分清洗,以减少二抗的非特异性结合。 二抗也可以在封闭溶液或清洗缓冲液中进行稀释。 如果制造商没有不同的指示,可以从1:200的稀释开始,在室温下孵育1小时。 有必要避光培养以防出现荧光色素漂白。
细胞核染色与样本封片
免疫反应之后通常是用DNA染料对细胞核染色。 另一方面,在用显微镜观察时这种处理可以更好地在细胞或组织切片内进行定向,同时还可以指示出细胞状态(如有丝分裂)是否为研究所需的状态。 即便在没有透化的情况下也能进入到细胞核并插入DNA中的染料,如Hoechst或DAPI等,可以用于此目的。 有鉴于此,实验人员应当十分小心,避免这些染料直接与皮肤接触! 室温下简单的细胞核染色耗时大约10分钟,期间Hoechst或DAPI需在PBS中稀释。
完成IF步骤后,样本必须适当封片以便于开展显微镜检查。 有鉴于此,需要使用封固介质(如Mowiol或Prolong Gold)将样本固定在显微镜载玻片上并防止样本脱水。 另外,封固介质增加了折射率,有利于使用油浸物镜进行显微镜检查。 一些制造商提供了带有添加剂的封固介质,如DABCO,这是一种防止样本光漂白的防褪色剂。 根据使用的荧光色素,一些抗褪色剂比其他的更有效。 此外,还可使用添加了DNA染料的封固介质以便在包埋期间对细胞核进行染色,就无需进行单独的细胞核染色。 如果使用硬化封固介质(通常情况下),则允许样本过夜固化,因此可以在第二天进行显微镜检查。 以这种方式生产的玻片几乎可以长时间储存在室温或4℃的黑暗环境中,但请记住,荧光色素的荧光强度会随着时间的推移而减弱。
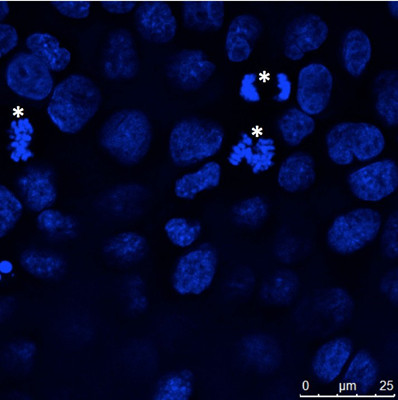
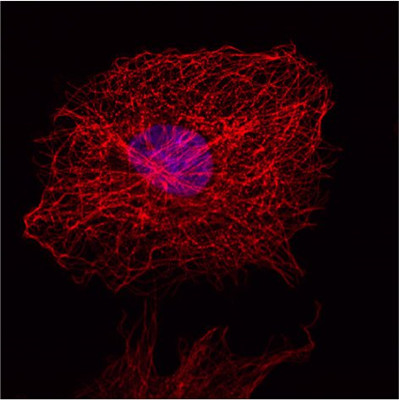
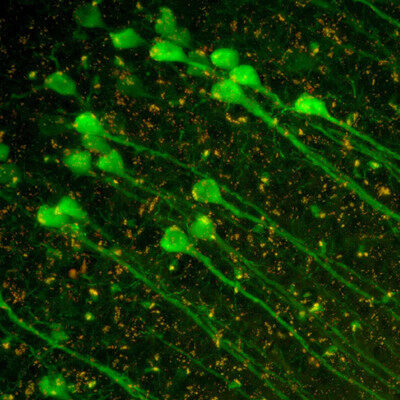
图 4: 贴壁生长的上皮细胞(MDCK)在盖玻片上培养、固定,细胞核用Hoechst 33342染色。 大多数细胞表现出间期DNA染色,但一些细胞出现染色体浓缩,这些染色体在有丝分裂中分离(星号)。 在徕卡TCS SP2上进行显微镜检查。
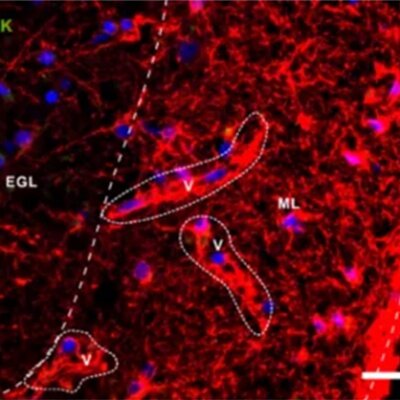
图 5: 该图展示了成纤维细胞(COS-7)当中细胞微管网状结构的间接IF染色。 细胞核使用Hoechst 33342进行染色并在Leica TCS SP2上开展显微镜检查。
对照
免疫荧光必须进行适当对照,以正确显示显微镜图像。 缺少或不适合的对照通常会导致假阳性结论和不正确的数据。 首先应当分析只被固定、透化和封闭的样本以便了解细胞间室的自发荧光typo3/。 有时即使没有进行IF染色,结构也可能出现强荧光信号。
为了进一步的对照和调整间接IF的显微镜参数,使用已采用上述方法进行处理过的样本,但样本还要额外使用二抗进行孵育。 首先将揭示二抗与样本的强非特异性结合。 其次,设置显微镜参数以便在该对照的图像采集期间不记录任何信号。 此设置用作后续采集的阈值来排除二抗的假阳性信号。 在直接IF当中,自体荧光对照用于调节阈值。 接下来分析与特异性一抗一起孵育的样本,如果是间接IF,也分析与二抗一起孵育的样本。 此时应可检测到荧光信号,其高于自发荧光和二抗的阴性对照。
为了确保一抗特异性标记所需结构,一些制造商为一抗提供可遮蔽特定抗原的肽封闭,从而防止抗体与其表位结合。 如此处理成本高昂,但也是确定抗体特异性的最佳方法,因此得到可靠的结果。 在多色IF实验中还必须注意所选荧光色素之间的串扰。 如果是第一次进行多色IF检查,建议在单独的制备中另外染色靶向结构,并将这些图像与多色图像进行比较。 最后应该仔细查看所获得的数据并将其与您的期望和一抗的现有数据进行比较。
| 对照 | 样本制备 | 适用于 |
| 自发荧光 |
| 分析细胞自发荧光。 直接IF的显微镜检查阈值。 |
| 二抗(仅限间接IF) |
| 二抗的非特异性结合。 间接IF中的显微镜检查阈值。 |
多色IF
|
| 比较信号染色与多色图像:
|
| 肽封闭 |
| 检查一抗与表位之间的结合特异性。 |
表 3: 哪些对照测试哪些内容?
局限性
如前所述,IF检查有诸多优势,但同样也存在着一定的劣势。 关键点是样本的固定: 固定意味着灭活,因此活细胞成像已变得不再可能。 因此对动态过程的分析会比较复杂,每个时间点上的细胞都必须予以固定和染色。 所以快速动态过程无法通过IF来进行观察。 这显然是融合蛋白表达荧光标记如GFP(绿色荧光蛋白)的优势,比较适合用于活细胞成像。 如上所述,IF实验过程中(固定/透化)会改变细胞结构,因此伪影可解释为假阳性信号。 所以有必要为每个IF染色准备适当的对照品,可能很费时。 另一个缺点同样不可避免:荧光染料的光漂白。 像GFP这样的荧光蛋白也受此影响,但当储存在适当的条件下,即使在几个月的永久性制备后,GFP也能被检测到。 相反,IF荧光色素的强度损失更快,这反映在显微镜下样本的快速漂白。 即使是用抗褪色剂封固介质也只能暂时起作用。
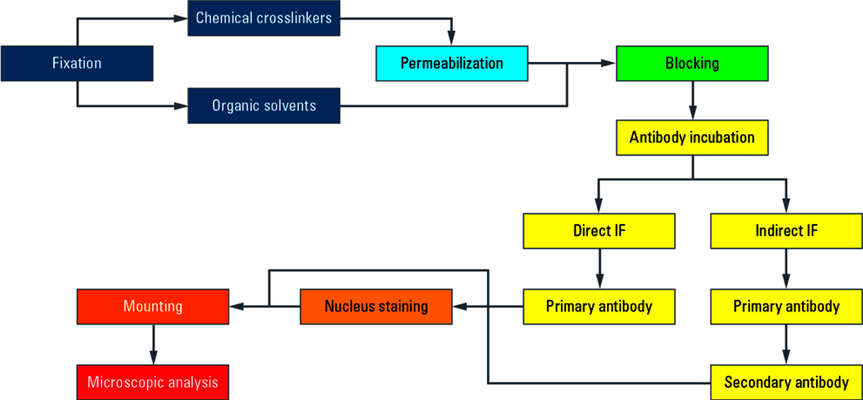
图 6: 整套程序的流程图。
标准IF流程
IF实验所需时间:约5个小时。
这是一种盖玻片上通过化学交联剂进行固定的培育细胞接受间接IF检查的标准方案。
- 湿盒非常适合IF实验,并且可以轻松完成自制(见幻灯片“如何制备湿盒”)。 该处理可防止试剂干燥并允许在黑暗中进行培养,这对于处理荧光色素很重要,并且对于已经存在的荧光蛋白是必要的。
- 试剂用量的选择要确保盖玻片能够完全湿润。 确保样本绝对不会完全干燥。
所有培育步骤都在室温下完成。
- 清洗细胞两次并使用镊子小心地将带有向上翻转细胞的盖玻片放入湿盒。
- 使用4%福尔马林进行10分钟的固定并清洗3次。
- 使用0.1% TX-100/PBS进行15-20分钟的透化处理并清洗3次。
- 使用5%正常山羊血清/PBS或1% BSA/PBS进行45分钟的封闭(无需清洗)。
- 在封闭溶液内稀释一抗并使用2小时(或在4℃下连夜使用)。 清洗4次将未结合的一抗彻底清除掉。
- 使用二抗进行1个小时的孵育,在封闭溶液或清洗缓冲液内进行稀释。
- 吸取二抗,如有需要可使用Hoechst或DAPI [1 μg/ML]在PBS中孵育10分钟。 彻底清洗4次,即便此时还没有出现细胞核染色。
- 用镊子轻轻取出盖玻片并将其浸入dH2O 内,清除掉清洗缓冲液的残留盐分。
- 在显微镜载玻片上滴一滴封固溶液并将盖玻片与细胞倒置这滴溶液上。 用镊子轻轻按压样本,使封固介质均匀分布而不会挤压样本。
- 固化后就准备好进行显微镜观察了。
配方
清洗缓冲液
1 × PBS(磷酸盐生理盐水缓冲液)
- 137 mM:NaCI
- 2.7 mM:KCI
- 10mM:Na2HPO4
- 1.8 mM:KH2PO4
- 使用HCI将pH值调节到7.2-7.4
- 如为PBS++,需添加最终浓度为1 mM的 CaCl2和MgCl2
- 如为PBS-T,需添加最终浓度为0.05%的Tween 20
固定缓冲液
福尔马林:
- 将4% PFA(多聚甲醛)溶解于温暖(50-70℃)的dH2O中,pH值8(使用NaOH进行调节)。将10 × PBS添加到最终浓度为1 × PBS的溶液中(如100 mL 10 × PBS溶于900 mL 4% PFA/dH2O)。
- 使用HCI将pH值调节到7.2-7.4。
- 甲醇(预先冷冻至-20℃):
100%甲醇(-20℃)
甲醇/丙酮(预先冷冻至 -20℃):
50%甲醇(-20℃)和50 %丙酮(-20℃)
透化缓冲液
TX-100(Triton X-100):
PBS,最终浓度0.1% TX-100
皂苷:
PBS,最终浓度0.1%的皂甙
其他清洁剂可在PBS中以相同浓度使用。
封闭缓冲液
BSA(牛血清白蛋白):
PBS,最终浓度为1% BSA
奶粉:
PBS,最终浓度为1%奶粉
正常血清:
PBS,最终浓度为5%正常血清
细胞核染料
Hoechst或DAPI:
在PBS中制备Hoechst 33342或DAPI溶液,最终工作浓度为1 μg/mL。"